La mole et les grandeurs molaires
-
1. المول وحدة كمية المادة :
-
1.1. تعريف المول :
المول هو كمية المادة لمجموعة تحتوي على عدد من المكونات الأساسية يساوي عدد الذرات الموجودة في 12g من الكربون
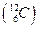 .
.
-
2.1. ثابتة أفوكادرو :
ثابتةأفوكادرو هي: NA=6,02.1023mol-1.
-
3.1. العلاقة بين كمية المادة وثابتة أفوكادرو :
بالنسبة لعينة من المادة X تحتوي على N من المكونات الأساسية تكون كمية مادة هذه العينة هي :
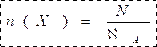
-
-
2. الكتلة المولية الذرية والكتلة المولية الجزيئية :
-
1.2. الكتلة المولية الذرية :
نسمي الكتلة المولية الذرية لعنصر كيميائي ، كتلة مول واحد من ذرات هذا العنصر .
-
2.2. الكتلة المولية الجزيئية :
نسمي الكتلة المولية الجزيئية لجسم خالص ، كتلة مول واحد من جزيئات هذا الجسم .
وتساوي مجموع الكتل المولية الذرية للذرات التي تدخل في تركيب الجزيئة
-
3.2. العلاقة بين كمية المادة والكتلة المولية :
تحدد كمية المادة n(X) ، لمادة X كتلتها m(X) بالعلاقة:
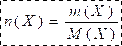
-
-
3. الحجم المولي للغاز :
-
1.3. تعريف :
نسمي الحجم المولي VM الحجم الذي يشغله مول واحد من غازات مختلفة في نفس الشروط لدرجة الحرارة والضغط
العلاقة بين كمية مادة الغاز وحجمه V والحجم المولي VM :
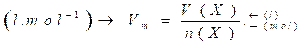
-
2.3. قانون أفوكادرو-أمبير :
تشغل نفس كمية مادة من غازات مختلفة في نفس الشروط لدرجة الحرارة والضغط نفس الحجم
بصيغة أخرى : عند نفس الظروف من درجة الحرارة والضغط، فإن أحجامًا متساوية من الغازات المختلفة تحتوي على عدد متساوٍ من الجزيئات
-
3.3. كثافة غاز بالنسبة للهواء :
هي النسبة بين كتلة حجم معين من غاز إلى كتلة نفس الحجم من الهواء،في نفس الشروط لدرجة الحرارة و الضغط
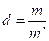
حيث m : كتلة حجم من الغاز . و m’ : كتلة نفس الحجم من الهواء .
عند الشروط النظامية :
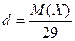
-
-
4. معادلة الغازات الكاملة :
-
1.4. متغيرات الحالة للغاز :
n كمية مادة الغاز و P ضغط الغاز و V حجم الغاز و T درجة الحرارة المطلقة
-
2.4. قانون بويل-ماريوط Loi de Boyle-Mariotte :
عند درجة حرارة ثابتة، يتناسب حجم كمية معينة من غاز عكسيا مع ضغطه
بصيغة أخرى : جداء حجم كمية معينة من غاز وضغطه يبقى ثابتا
T=cte ==> P.V=cte
-
3.4. الغاز الكامل :
الغاز الكامل هو كل غاز يخضع خضوعا تاما لقانون بويل – ماريوط و قانون أفوكادرو – أمبير
-
4.4. معادلة الحالة للغاز الكامل :
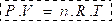
حيث :
- n : كمية مادة الغاز بالمول (mol)
- P: ضغط الغاز بالباسكال (Pa)
- V: حجم الغاز ب (m3)
- T : درجة الحرارة المطلقة بالكلفن (K) :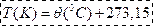
- R : ثابتة الغازات الكاملة . قيمة R :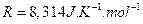 أو
أو 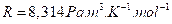 .
.
-