Concentration molaire des espèces moléculaires dans une solution
1. تعريف محلول مائي :
يتم الحصول على المحلول عن طريق إذابة نوع كيميائي في سائل يسمى مذيب: الأنواع الكيميائية المذابة تسمى مذاب.
في المحلول ، المذيب هو غالبية الأنواع الكيميائية والمذاب هو الأقلية.
هناك حد لقابلية ذوبان الأنواع الكيميائية في مذيب: إذا تم تجاوز هذا الحد ، يتم الحصول على محلول مشبع.
ملحوظة :
إذا كان المذيب هو الماء ، فإن المحلول يسمى محلول مائي.
2. مفهوم التركيز :
1.2. مفهوم التركيز الكتلي :
نسمى التركيز الكتلي Cm(X) النسبة (قسمة) كتلة المذاب X مذابة m(X) الى (على) الحجم الكلي المحلول Vs :
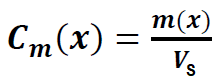
يعبر عن التركيز الكتلي ب g/L.
2.2. مفهوم التركيز المولي :
نسمى التركيز المولي C(X) لمذاب في محلول مائي لهذا المذاب , النسبة (قسمة) n(X) كمية المادة المذابة الى (على) الحجم الكلي المحلول Vs :
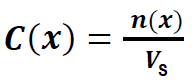
غالبًا ما يتم التعبير عن التركيز المولي ب mol/L وهي ليست وحدة دولية. الوحدة الدولية للتركيز المولي هي mol/m3
-
3.2. العلاقة بين التركيز المولي والتركيز الكتلي :
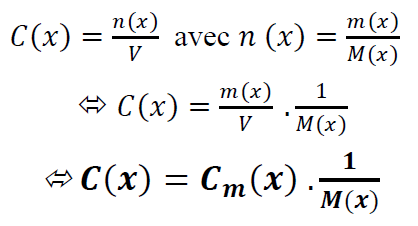
3. تخفيف محلول مائي :
-
1.3. تعريف :
تخفيف محلول مائي هو إضافة الماء المقطر إلى حجم معين من هذا المحلول: :
- يسمى المحلول في البداية المحلول الأم (البدئي).
- يسمى المحلول المخفف الذي تم الحصول عليه بالمحلول الابن.
التركيز المولي Cfille للمحلول الابن دائما أقل من التركيز المولي Cmère للمحلول الأم
-
2.3. علاقة التخفيف :
أثناء التخفيف ، يتم انحفاظ كمية المادة المذابة nfille=nmère , مما ينتج عنه علاقة بين التركيزات Cfille و Cmère و الاحجام Vmère و حجم محلول الأم المأخوذ و Vfille حجم المحلول الابن الناتج ;
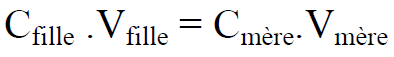
-
3.3. تحضير المحلول عن طريق التخفيف :
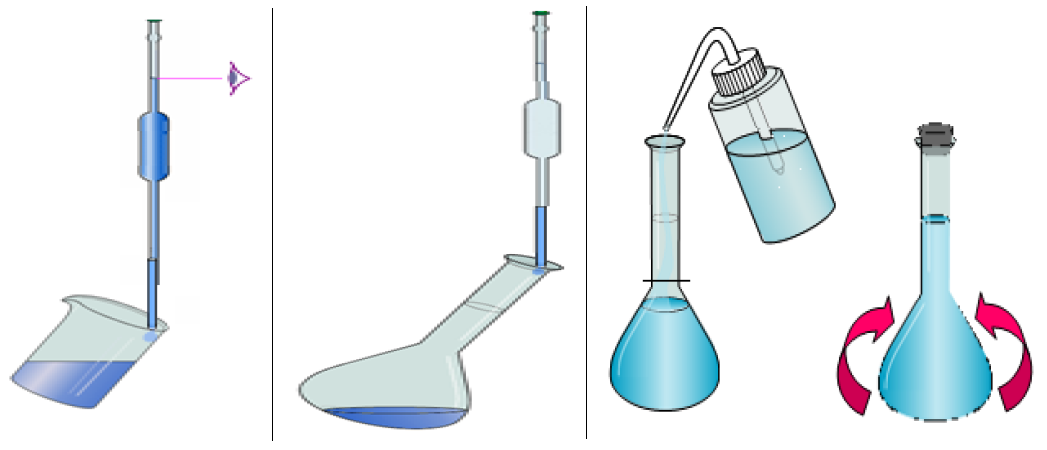
* أدخل المحلول الأم في دورق.
* باستخدام ماصة تمت معايرتها وشطفها وبحجم محسوب مسبقًا ، خذ المحلول الأم .
* صب المحلول الأم الذي تم أخذ عينات منه في دورق حجمي بحجم مناسب.
* املأ الحوجلة المعيارية بالماء المقطر حتى العلامة ورجها عن طريق قلب الحوجلة المعيارية تمامًا لتجانس المحلول.
-