المعايرة المباشرة
1. Principe de dosage direct :
1.1. Définitions :
Le dosage d'un produit chimique de type A de concentration inconnue (le titrant) consiste à adopter une réaction chimique qui se produit entre lui et un autre produit chimique de type B qui apporte une autre solution de concentration connue (le titrant).
La réaction entre A et B est appelée réaction de dosage et doit répondre aux conditions suivantes:
* Totale (ou complète) : le réactif limitant est totalement épuisé.
* Rapide : l'interaction se termine instantanément ou dans une courte durée.
* Sélective : le titrant B ne réagit qu'avec le titré de type A.
Avec l'ajout du titrant B, le titrant A continue à être consommé jusqu'à ce que le titrant A ne soit plus consommé, auquel cas les réactifs A et B sont tous les deux consommés. On dit que le dosage a atteint le point d'équivalence, et on appelle le volume ajouté du titrant pour atteindre l'équivalence, le volume à l'équivalence, et on le note : Véq.
2.1. Déterminer la concentration inconnue :
On considère l'équation de dosage suivante: aA + bB
 cC + dD
cC + dD Créons le tableau descriptif:
* avant l'équivalence
état de la reaction
avancement de la reaction
aA + bB
 cC + dD
cC + dD Etat initial
x=0
0
0
ni(B)
ni(A)
pendant la reaction
x
d.x
c.x
ni(B)-b.x
ni(A)-a.x
état final
x=xmax
d.xmax
c.xmax
0
ni(A)-a.xmax
* à l'équivalence
état de la reaction
avancement de la reaction
aA + bB
 cC + dD
cC + dD Etat initial
x=0
0
0
ni(B)
ni(A)
pendant la reaction
x
d.x
c.x
ni(B)-b.x
ni(A)-a.x
état final
x=xmax
d.xmax
c.xmax
0
0
* après l'équivalence
état de la reaction
avancement de la reaction
aA + bB
 cC + dD
cC + dD Etat initial
x=0
0
0
ni(B)
ni(A)
pendant la reaction
x
d.x
c.x
ni(B)-b.x
ni(A)-a.x
état final
x=xmax
d.xmax
c.xmax
ni(B)-b.xmax
0
* exploitation du tableau descriptif: à l'équivalence
A l'état final de la réaction on a: nf(A)=nf(B)=0
donc: ni(A)-a.xmax= ni(B)-b.xmax=0
On sait que : ni(A)=CA.VA et ni(B)=CB.VBéq
 CA.VA-a.xmax=0 et CB.VBéq-b.xmax=0
CA.VA-a.xmax=0 et CB.VBéq-b.xmax=0 
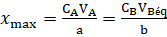
alors:
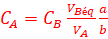
2. Méthodes du dosage direct :
1.2. dosage par conductimétrie - Application :
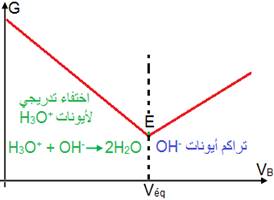
On trace l'évolution de la poursuite d'une portion d'une solution aqueuse d'acide chlorhydrique, de concentration inconnue CA en fonction du volume ajouté VB d'une solution aqueuse de soude, de concentration connue en CB , on obtient donc la courbe suivante :
De la courbe on obtient le point d'équivalence E, et donc le volume ajouté à l'équivalence est : Véq.
* Calculons la concentration CA
état de la reaction
avancement de la reaction
H3O+ + OH-
 2H2O
2H2O Etat initial
x=0
en excès
ni(OH- )
ni(H3O+ )
pendant la reaction
x
en excès
ni(OH- )- x
ni(H3O+ )-x
état final
x=xmax
en excès
ni(OH- )- xmax
ni(H3O+ )-xmax
à l'équivalence: ni(H3O+ )-xmax=0 et ni(OH- )- xmax=0
 CA.VA=xmax et CB.VBéq=xmax
CA.VA=xmax et CB.VBéq=xmaxdonc:
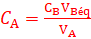
2.2. dosage colorimétrique :
nous titrons une solution de sulfate de fer II, de concentration inconnue C1, par une solution de permanganate de potassium de concentration connue C2.
Dans un premier temps, la couleur violette de permanganate disparaît après mélange avec du sulfate de fer II, car elle se transforme en ions manganèse Mn2+ incolores , selon l'équation suivante :
MnO4- + 5Fe2+ + 8H+
 Mn2+ + 5Fe3+ + 4H2O
Mn2+ + 5Fe3+ + 4H2O Lorsque tous les ions Fe2+ sont consommés, les ions MnO4- ne réagissent pas - ce qui explique la coloration du mélange..
* Calculons la concentration inconnue C1
état de la reaction
avancement de la reaction
MnO4- + 5Fe2++ 8H+
 Mn2+ + 5Fe3+ + 4H2O
Mn2+ + 5Fe3+ + 4H2OEtat initial
x=0
en excès
0
0
en excès
ni(Fe2+ )
ni(MnO4- )
pendant la reaction
x
en excès
5.x
x
en excès
ni(Fe2+ )-5.x
ni(MnO4- )- x
état final
x=xmax
en excès
5.xmax
xmax
en excès
ni(Fe2+ )-5.xmax
ni(MnO4- )- xmax
A l'équivalence: ni(MnO4- )- xmax=0 et ni(Fe2+ )-5.xmax=0
 C1V1=5.xmax et
C2V2éq=xmax
C1V1=5.xmax et
C2V2éq=xmaxdonc:
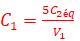
3. Précision de dosage
La précision de l'étalonnage dépend de la précision de chaque mesure donnée, C2, V1, V2éq.
* Par example :
* Précision de C2: Elle dépend de la méthode utilisée. Considérons C2m=0.030mol.L-1 , et la précision est : ± 0.001 mol.L-1.
* Précision de V1: en rapport avec la précision de la pipette standard. Considérons V1m=20.00mL , et la précision est: ± 0.02mL .
* Précision de V2éq: liée à la précision de la burette. Considérons V2éqm=13.30mL , et la précision est: ± 0.05mL .
+ Calculons l'intervale de la précision de la concentration C1
On a :
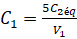
 C1m=0.10mol.L-1
C1m=0.10mol.L-1La précision est la somme des précisions: ± 0.07mol.L-1
Ainsi : 0.3 mol.L-1 ≤ C1≤ 0.17 mol.L-1