نموذج الذرة
1. STRUCTURE DE L’ATOME :
L’atome est constitué d’un noyau et d’électrons.
1.1. Les électrons :
Un électron est de masse est me = 9,1.10-31kg Et sa charge électrique qe = –e = -1,6.10-19C.
1.2. Le noyau :
Il est constitué de particules élémentaires : les protons et les neutrons désignés sous le nom de nucléons:
* Les protons
ils sont chargés positivement : e=+1,6.10-19C, et de masse très petite mp=1,7.10-27kg.
* Les neutron
ils sont des particules neutres électriquement, et ils ont une masse voisine de celle du proton donc: mn=1,7.10-27kg
1.3. Les nombres Z, N et A :
Le nombre de protons du noyau s’appelle nombre de charge ou numéro atomique et se note Z.
Le nombre de neutrons se note N.
Le nombre total de nucléons ou nombre de masse, noté A est tel que : A = Z + N
Remarque :
Un atome étant électriquement neutre, il possède autant de protons que d’électrons.
1.4. Symboles :
Un atome est symbolisé par une ou deux lettres. La première s’écrit toujours en majuscule et la deuxième en minuscule. Le symbole correspond souvent au début du nom de l’atome mais certains sont issus du nom latin :
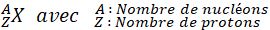
Exemple :
Le noyau de SODUIM
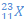
Nombre de nucléons
Nombre de protons
Nombre de neutrons
Nombre des électrons
A=23
Z=11
N=A-Z=12
N e =Z=11
1.4. Masse de l’atome :
La masse de l’atome est la somme de la masse de ses différents constituants :
matome= mnoyau + mélectrons = (Z.mp + N.mn ) + Z.me
Si on néglige la masse des électrons devant celle des protons (Soit mp/me = 1835) alors la masse approchée de l’atome est égale à : matome = Z.mp + N.mn = A.mnucléon
La masse de l’atome est concentrée dans son noyau et déponde de A Ce nombre s’appelle nombre atomique.
Exemple ;
Noyau de CARBONE 126C
m(126C)=12.mp=20,4.10-27Kg
2. ISOTOPES
Des isotopes sont des atomes ayant par le même numéro atomique Z et des nombres de nucléons A différents (Ils diffèrent par leur nombre de neutrons).
Exemple :
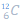 ;
;
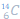 Isotope de carbone (Il y a 2 neutrons de plus dans le 2ème)
Isotope de carbone (Il y a 2 neutrons de plus dans le 2ème)3. IONS MONOATOMIQUE :
Un ion monoatomique est un atome qui a perdu ou gagné un (ou plusieurs) électron(s). Le noyau n’est pas modifié.
Un atome et l'ion monoatomique ont donc le même nombre Z de protons et le même nom, le même symbole.
- Un atome est électriquement neutre. S’il perd des électrons (négatifs), il devient chargé positivement, c’est un ion positif. Exemple Na +
- Si un atome gagné des électrons (négatifs), il devient chargé négativement, c’est un ion négatif. Exemple : Cl -
4. STRUCTURE ELECTRONIQUE D’UN ATOME
4.1. Les couches électroniques :
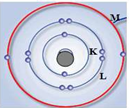 Les électrons sont en mouvement autour du noyau : on parle de « cortège électronique » du noyau.
Les électrons sont en mouvement autour du noyau : on parle de « cortège électronique » du noyau.Les électrons d’un atome se répartissent dans des couches électroniques. Chaque couche est représentée par une lettre ; pour les atomes dont le numéro atomique est inférieur à 19, les couches occupées sont les couches K, L et M.
La dernière couche occupée s’appelle la couche externe.
Les électrons qui l’occupent sont appelés les électrons périphériques de l’atome
4.2. Règles de remplissage :
Une couche électronique ne peut contenir qu’un nombre limité d’électrons
Couche
K
L
M
Nombre d’électrons
2
8
8
- Une couche contenant un nombre maximal d’électrons est dite saturée.
- Les électrons commencent par occuper la couche K puis la L et enfin la M. Ils ne peuvent se placer sur une nouvelle couche si la précédente n’est pas pleine.
Le résultat de la répartition des électrons se nomme la structure électronique de l’atome.
4.3. Représentation de la structure électronique
La structure électronique est composée des lettres correspondant aux couches K,L,M. Les lettres sont écrites entre parenthèse. On indique le nombre d’électrons qu’elles contiennent en exposant haut à droite.
Exemple :
- L’atome d’oxygène 8 O a pour numéro atomique Z = 8. Le nombre d’électrons est 8 puisque l’atome est électriquement neutre. La structure électronique de cet atome se note : (K) 2 (L) 6
- L’atome de chlore 17 Cl a pour numéro atomique Z = 17. Sa structure électronique est : (K) 2 (L) 8 (M) 7
- L’ion de chlore 17 Cl - a pour numéro atomique Z = 17+gagne un électron ; Sa structure électronique est : (K) 2 (L) 8 (M) 8
- Ion aluminium Al 3+ : Z = 13 . Il y a 13 protons dans le noyau. Un atome d’aluminium possède donc 13 électrons, autant que de protons. L’ion Al 3+ a une charge 3+, il a perdu 3 électrons, il a donc 10 électrons. Formule électronique : (K) 2 (L) 8