Transformations spontanées dans les piles et récupération d'énergie
1. الانتقال التلقائي للإلكترونات :
1.1. الانتقال التلقائي المباشر ( بين أنواع كيميائية مختلفة ) :
في حالة وجود المؤكسد و المختزل في نفس الوسط فأن انتقال الالكترونات يتم بطريقة مباشرة
1.2. الانتقال التلقائي للإلكترونات بين أنواع كيميائية منفصلة:
في حالة عجم وجود المؤكسد و المختزل في نفس الوسط فأن انتقال الالكترونات يتم بواسطة تربط المختزل بالمؤكسد: انتقال بطريقة غير مباشرة
2. مكونات عمود :
- العمود مولد كهربائي يحول الطاقة الكيميائية الناتجة عن تفاعل أكسدة-اختزال تلقائي ، إلى طاقة كهربائية.
- يتكون عمود من نصفي عمود (نسمي نصف عمود مجموعة متكونة من سلك ( أو صفيحة ) من فلز
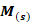 ، يُدعى إلكترودا ، مغمور في محلول إلكتروليتي يحتوي على الأيونات
، يُدعى إلكترودا ، مغمور في محلول إلكتروليتي يحتوي على الأيونات 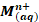 ) مرتبطين كهربائيا بواسطة قنطرة ملحية ( أيونية ) يحتوي كل نصف عمود على مؤكسد و مختزل مزدوجة.
) مرتبطين كهربائيا بواسطة قنطرة ملحية ( أيونية ) يحتوي كل نصف عمود على مؤكسد و مختزل مزدوجة. 3. مبدأ اشتغاله
1.3. مبدأ اشتغال عمود : عمود دنيال مثلا
النصف الاول للعمود
على مستوى القطب السالب للعمود : الانود (- )
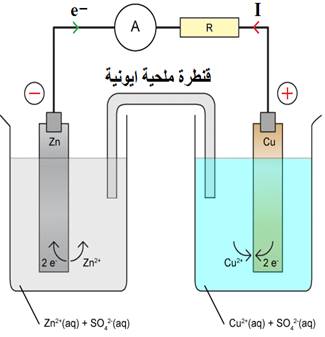 تحدث نصف المعادلة: اكسدة فيؤدي هذا الى :
تحدث نصف المعادلة: اكسدة فيؤدي هذا الى : - تكون ايونات كاتيونات : أي زيادة عدد الشحن الموجبة
- تحرير الالكترونات تنتقل عبر السلك فتصل الى النصف الثاني للعمود
- فائض في الشحن الموجبة و نقص في الشحن السالبة
النصف التاني للعمود
على مستوى القطب الموجب للعمود : الكاتود (+ )
تحدث نصف المعادلة: اختزال فيؤدي هذا الى :
- استهلاك ايونات كاتيونات : أي انخفاض عدد الشحن الموجبة
- استهلاك الالكترونات التي تصل من النصف الاول للعمود
- فائض في الشحن السالبة و نقص في الشحن الموجبة
القنطرة الملحية الايونية
تسمح القنطرة الملحية بربط نصفي العمود فتضمن الحياد الكهربائي حيث تتساوى عدد الشحن الموجبة مع عدد الشحن السالبة.
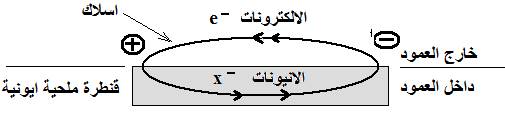
2.3. تحديد قطبية العمود
الطريقة 1: بواسطة جهاز الامبيرمتر ( او الفولطمتر ) حيث اذا اشار الجهاز الى قيمة موجبة فهذا يعني ان قطبه السالب COM مرتبط بالقطب السالب للعمود، اما اذا اشار الجهاز الى قيمة سالبة فهذا يعني ان قطبه السالب COM مرتبط بالقطب الموجب للعمود
الطريقة 2: باعتماد الملاحظات التجريبية الصفيحة التي يلاحظ فيها التأكل يعني انها تعرضت لعملية الاكسدة أي تمثل القطب السالب للعمود و على الصفيحة التي يلاحظ فيها التوضع يعني ان تفاعل الاختزال حدث بجانبها أي تمثل القطب الموجب للعمود
الطريقة 3 : باعتماد معيار التطور التلقائي حيث يتم تحديد المنحى الحقيقي لتطور المجموعة الكيميائية و عندها يتم تفكيك المعادلة إلى نصفين فالأكسدة توافق القطب السالب و الاختزال يوافق القطب الموجب .
3.3. التمثيل الاصطلاحي لعمود
نعتبر عمودا مكونا من المزدوجتين
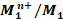 و
و 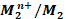 حيث
حيث 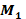 القطب (-) و
القطب (-) و 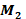 القطب (+) .
القطب (+) . بصفة عامة التبيانة الاصطلاحية لهذا العمود هي :
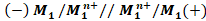 و يشير الخطان الموزيان // الى قنطرة ملحية ايونية
و يشير الخطان الموزيان // الى قنطرة ملحية ايونية مثال عمود دنيال :
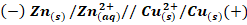
4. الدراسة الكمية لعمود
1.4. كمية الكهرباء
Û نسمي كمية الكهرباء
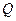 المستعملة خلال اشتغال عمود لمدة
المستعملة خلال اشتغال عمود لمدة 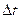 ، القيمة المطلقة للشحنة الكلية للإلكترونات المتبادلة خلال هذه المدة : Q=N.e
، القيمة المطلقة للشحنة الكلية للإلكترونات المتبادلة خلال هذه المدة : Q=N.e حيث N عدد الالكترونات المتبادلة خلال
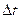 مدة اشتغال العمود و e الشحنة الابتدائية للالكترون
مدة اشتغال العمود و e الشحنة الابتدائية للالكترون مع N=n(e-).NA اي
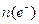 : كمية مادة الإلكترونات المتبادلة نستنتج ان : Q= n(e-).NA.e
: كمية مادة الإلكترونات المتبادلة نستنتج ان : Q= n(e-).NA.e مع الكمية : F= NA.e تسمى ثابتة فردي وتمثل شحنة 1 مول من الالكترونات
Û إذا كانت الشدة I للتيار المار في الدارة ثابتة خلال مدة
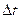 ، نكتب :
، نكتب : 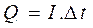
و بالتالي:
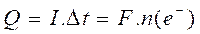
2.4. كمية الكهرباء القصوى الممكن تمريرها من طرف عمود:
عندما يصل العمود إلى حالة التوازن ، تتوقف كميات الأنواع المتدخلة عن التطور ، فلا يحدث إي تفاعل على مستوى الإلكترودين و بالتالي ليس هناك انتقال للإلكترونات عبر الدارة الخارجية : لم يعد بإمكان العمود توليد التيار ،
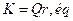 و
و 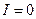 .
. "يكون العمود عند التوازن ، مُستَهلكا ليس بإمكانه توليد التيار الكهربائي".
كمية الكهرباء القصوى الممكن تمريرها من طرف عمود أي سَعَة العمود:
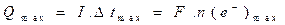
حيث
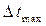 : مدة حياة العمود .
: مدة حياة العمود . 3.4. كمية الكهرباء و تقدم التفاعل خلال مدة اشتغال العمود Δt
الجدول الوصفي لاحد انصاف المعادلتين
Red ⇄ Ox + n e-
0
n 0 (Ox)
n 0 (Red)
عند t=0
n .x(t)
n0(Ox)+x(t)
n0(Red)-x(t)
عند t
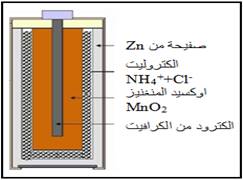
من خلال الجدول جانبه n(e-)=n.x(t) حيث n يمثل عدد الالكترونات
Q= n.x(t).F
اي x(t)=
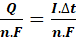
5. أمثلة لأعمدة اعتيادية
1.5. العمود الملحي : لوكلانشي :
- تسمى بالملحية لكون إكتروديها مغمورين في محلول مخَتَّر لكلورور الأمونيوم NH4 + +Cl - ) و كلورور الزنك ( .
- المعادلة المعبرة عن اشتغالها
Zn+2MnO2+2H+ ⇄ Zn2++2MnO(OH)
- التمثيل الاصطلاحي:
(-) Zn/Zn 2+ // MnO(OH)/MnO 2 /C (+)
2.5. العمود القلائــــي :
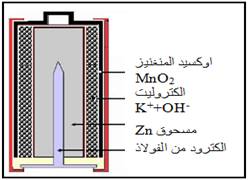
- نفس مكونات العمود الملحي تقريبا غير ان الإلكترودان مغموران في محلول قاعدي مخَتَّر لهيدروكسيد البوتاسيوم (K++OH- ) ، و تسمى قلائية بسبب عنصر البوتاسيوم.
- المعادلة المعبرة عن اشتغالها:
Zn+2MnO2+2OH-+2H2O ⇄ Zn(OH)42-+2MnO(OH)
- التمثيل الاصطلاحي:
(-)Zn/Zn(OH)42-//MnO(OH)/MnO2/acier (+)
3.5. عمود ذو محروق :
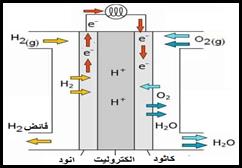
مثل الأعمدة بثنائي الهيدروجين و ثنائي الأوكسجين
- يصل H2 إلى الأنود فيتأكسد
- و يصل O2 إلى الكاثود فيختزل
الإلكتروليت المستعمل يمثل قنطرة ايونية و يكون إما قلائي (K++OH-) او حمضيا مثل (حمض الفوسفوريك)
معادلة اشتغال العمود
2H2 + O2 ⇄ 2H2O