Réactions d'estérification et d'hydrolyse
1. تفاعل الاسترة :
1.1. تعريف :
تفاعل الاسترة هو تفاعل يحدث بين حمض كربوكسيلي وكحول خلاله يفقد الحمض الكربوكسيلي المجموعة (-OH) اما الكحول فيفقد (-H) وبذلك تتحد الجزيئتان لاعطاء استير و جزيئة الماء وفق المعادلة التالية :
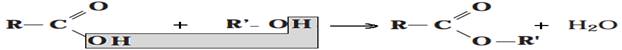
1.2. مميزات تفاعل الاسترة :
تفاعل لاحـــــراري : اي ان المجموعة لا تتبادل الحرارة مع الوسط الخارجي
تفاعل بطـــــــــــيء: يستلزم وقت طويل للوصول الى حـــــــــــــــده (ساعات .... )
تفاعل محـــــــــدود : يصل الى النهاية مع تواجد المتفاعلات معــــــــــــــــــــا
2. تفاعل الحلمأة
2.1. تعريف :
- هو تفاعل يحدث بين الاستير و الماء اي في المنحى المعاكس لتفاعل الاسترة وفق المعادلة التالية

2.2. مميزات تفاعل الحلمـــأة
تفاعل لاحـــــراري : اي ان المجموعة لا تتبادل الحرارة مع الوسط الخارجي
تفاعل بطـــــــــــيء: يستلزم وقت طويل للوصول الى حده
تفاعل محـــــــــدود : يصل الى النهاية مع تواجد المتفاعلات معا
3. التوازن أسترة ــ حلمأة
- إن تفاعلي الأسترة والحلمأة متزامنان ويحدثان في منحيين متعاكسين.
- بصفة عامة نعبر عن التوازن أسترة ـ حلمأة بالمعادلة
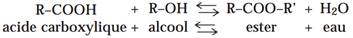
يلعب الماء دور متفاعل في الحلمأة و ناتج في الاسترة و ليس مذيبا اذن :
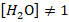
- تعبير خارج التفاعل لتفاعل الاسترة
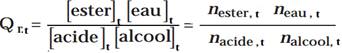
- تابتة التوازن لتفاعل الاسترة تعبير
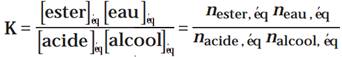
عند انطلاق من خليط متساوي المولات n0 من الحمض و n0 من الكحول فأننا عند التوازن نحصل على كمية مادة الاستير حسب نوع الكحول المستعمل
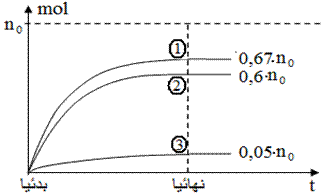
كحول اولي 1, كحول ثانوي 2, كحول ثالثي 3
4. التحكم في تحول كيميائي
قصد الوصول الى الحالة النهائية في مدة اقل لابد من رفع سرعة تطور المجموعة الكيميائية
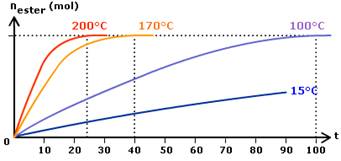
4.1. برفع درجة الحرارة
يؤدي ارتفاع درجة حرارة المجموعة الكيميائية الى تسريع تطورها
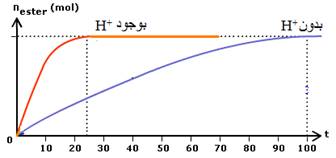
4.2. باضافة الحفاز :
الحفاز نوع كيميائي يرفع من سرعة التفاعل دون أن يتدخل في معادلة التفاعل
يؤدي وجود الحفاز الى تسريع تطور المجموعة الكيميائية
5. مردود تحول كيميائي
5.1. تعريف المردود
يساوي المردود r لتفاعل كيميائي، خارج كمية المادة nexp المحصلة تجريبيا على كمية المادة nth المنتظر الحصول عليها باعتبار التحول كلي، ونكتب r=
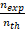 ومعرفة قيمته تمكن من تقيم فعالية التحول.
ومعرفة قيمته تمكن من تقيم فعالية التحول. 5.2. بعض طرق رفع المردود
للرفع من مردود تصنيع الاستير مثلا نقوم :
- باستعمال احد المتفاعلات (حمض او كحول ) بوفرة
- ازالة احد النواتج (الماء او الاستير المتكون) حيث نمنع التحول في المنحى المعاكس