Contrôle de l'évolution d’un système chimique
-
1. لماذا تغيير متفاعل
خلال كل عملية تصنيع يراعى ما يلي :
* ان تكون مردودية التصنيع مرتفعة مع الحفاظ على الطاقة و المواد الاولية .
* ان تكون تكلفة الانتاج منخفضة
* السرعة في الانتاجية
لهذه الاسباب ... لابد من توفير الظروف المناسبة و ذلك بتغيير متفاعلات أو إضافات حفازات أو ...
-
2. التحكم في تطور المجموعة الكيميائية بتغيير متفاعل
-
1.2. تصنيـع استيــر
يتميز تصنيع الاستيرات انطلاقا من حمض كربوكسيلي و كحول بأنها تفاعلات بطيئة و غير كلية و تؤذي الى تكون الماء فتتم حلمأة الاستير، لهذا السبب نقوم بتغيير متفاعل حيث تتكون نواتج لا تتفاعل فيما بينها فنمنع التحول في المنحى المعاكس
à نعوض الحمض الكربوكسيلي بأحد مشتقاته مثل اندريد الحمض الكربوكسيلي
معادلة التحول
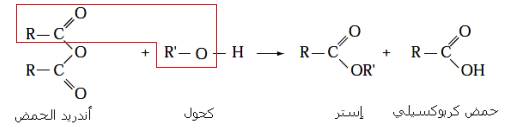
* تتميز هذه التفاعلات بأنها سريعة و تامة (كلية)
* يتم هذا التفاعل في وسط لامائي تفاديا لتفكك اندريد الحمض و منع حدوث تفاعل الحلمأة
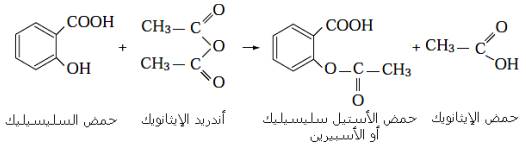
$ مثال : يتم تحضير الاسبيرين انطلاقا من اندريد الايثانويك و حمض 2- هيدروكسيبنزويك (يتوفر على المجموعة OH ) و ذلك تحث درجة حرارة 60°- 90° و باستعمال حفاز ( H2SO4 ) حسب المعادلة التالية :
-
2.2. الحلمأة القاعــــدية للاستيـــــرات : التصبـــــن
تتميز حلمأة الاستيرات بوجود الماء بأنها تفاعلات بطيئة و غير كلية و يؤذي الى تكون الحمض و الحول فتحدث الاسترة ، لهذا السبب نقوم بتغيير متفاعل فنعوض الماء بقاعدة قوية مثل ( Na++ OH- ) أو ( K+ +OH- )، وفق المعادلة التالية :
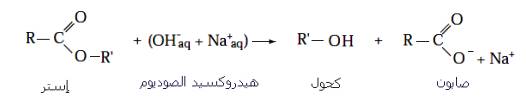
الناتج : كربوكسيلات الصوديوم R-COO- + Na+ هو الصابون
-
3.2. تصبن الاجسام الدهنية (الحلمأة القاعدية ) : تحضير الصابون
الاجسام الدهنية عبارة عن ثلاتية الاستير و هي نتيجة تفاعل الاسترة بين حمض دهني و الغليسيرول
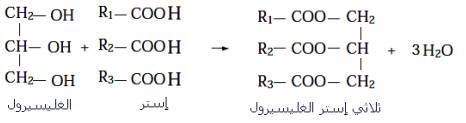
يتم تحضير الصابون بتصبن الاجسام الدهنية ( السائلة و الصلبة ) و التي تحتوي المجموعات المميزة استير ، وفق المعادلة التالية :
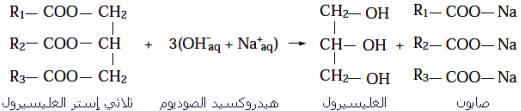
ملحوظة: في حالة استعمال ( Na++ OH- ) نحصل على صابون صلب و في حالة استعمال ( K+ +OH- ) نحصل على صابون ليـــــن
تأثير الصابون على الاوساخ :
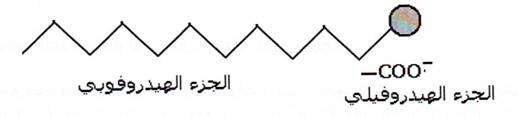
تتكون جزيئة الصابون ( أيون الكربوكسيلات R-CO2- ) على جزئين :
* راس –CO2- : محبة للماء ( هيدروفيلية hydrophile ) و كارهة للدهنيات (ليبوفوبية Lipophobe ).
* ذيل -R : كارهة للماء ( هيدروفوبية hydrophobe ) و محبة للدهنيات (ليبوفيلية Lipophile ) .
عند وضع توب ملطخ ببقعة دهنية في ماء صابوني فإن الاجزاء المحبة للذهون تتجمع حول البقعة الزيتية
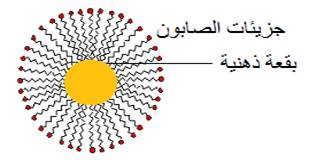
فبعد عملية الفرك تنفصل البقع الدهنية المحاطة بجزيئات الصابون عن التوب فتتشتت في الماء
-
3. التحكم في تطور مجموعة كيميائية بالحفز:
-
1.3. تعريف الحفاز
الحفاز نوع كيميائي انتقائي و نوعي لا يغير حالة التوازن و إنما يزيد من سرعة التفاعل.
-
2.3. أنواع الحفز
· الحفز المتجانس: عندما يكون الحفاز والمتفاعلات ينتميان لنفس الطور.
· الحفز الغير المتجانس: عندما يكون الحفاز والمتفاعلات لا ينتميان لنفس الطور.
· الحفز الأنزيمي: عندما يكون الحفاز أنزيما. وهو يشمل عدة فجوات تعتبر مواقع فعالة تثبث المتفاعلات و تزيد من سرعة تفاعلها
-
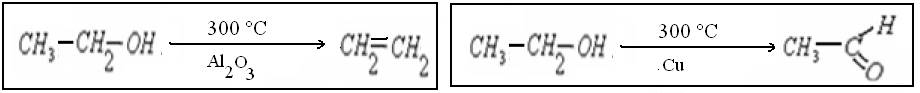
3.3. انتقائية الحفاز
يوجه الحفاز التحول الكيميائي اي ان التحول يمكنه ان يتطور في اتجاة مختلف حسب الحفاز المستعمل