Le dosage direct
1. مبدأ المعايرة المباشرة :
1.1. تعاريف :
معايرة نوع كيميائي A مجهول التركيز ( المحلول المعايَر ) تكون باعتماد تفاعل كيميائي يحدث بينه وبين نوع كيميائي آخر B يأتي به محلول آخر ذو تركيز معروف ( المحلول المعايِر ).
التفاعل الحاصل بين A و B يسمى تفاعل المعايرة , ويجب أن تتوفر فيه الشروط التالية:
* كليا أو تاما: يُستهلك المتفاعل الحدي كليا.
* سريعا: ينتهي التفاعل لحظيا أو في وقت وجيز.
* انتقائيا: لا يتفاعل النوع المعايِر B إلا مع النوع المعايَر A .
مع إضافة المحلول المعايِر B يتواصل استهلاك المتفاعل المعايَر A حتى تنعدم كمية مادته, في هذه الحالة يكون قد تم استهلاك المتفاعلان A و B معا. نقول إن المعايرة وصلت إلى نقطة التكافؤ , ونسمي الحجم المضاف من المحلول المعايِر للوصول إلى التكافؤ, الحجم عند التكافؤ , ونرمز له ب: Véq.
2.1. تحديد التركيز المجهول
نعتبر معادلة المعايرة التالية: aA + bB
 cC + dD
cC + dD لننشئ الجدول الوصفي:
* قبل التكافؤ
حالة التفاعل
تقدم التفاعل
aA + bB
 cC + dD
cC + dD الحالة البدئية
x=0
0
0
ni(B)
ni(A)
أثناء التفاعل
x
d.x
c.x
ni(B)-b.x
ni(A)-a.x
الحالة النهائية
x=xmax
d.xmax
c.xmax
0
ni(A)-a.xmax
* عند التكافؤ
حالة التفاعل
تقدم التفاعل
aA + bB
 cC + dD
cC + dD الحالة البدئية
x=0
0
0
ni(B)
ni(A)
أثناء التفاعل
x
d.x
c.x
ni(B)-b.x
ni(A)-a.x
الحالة النهائية
x=xmax
d.xmax
c.xmax
0
0
* بعد التكافؤ
حالة التفاعل
تقدم التفاعل
aA + bB
 cC + dD
cC + dD الحالة البدئية
x=0
0
0
ni(B)
ni(A)
أثناء التفاعل
x
d.x
c.x
ni(B)-b.x
ni(A)-a.x
الحالة النهائية
x=xmax
d.xmax
c.xmax
ni(B)-b.xmax
0
* استثمار الجدول الوصفي: عند التكافؤ
في الحالة النهائية للتفاعل لدينا: nf(A)=nf(B)=0
أي: ni(A)-a.xmax= ni(B)-b.xmax=0
نعلم أن: ni(A)=CA.VA و ni(B)=CB.VBéq
 CA.VA-a.xmax=0 و CB.VBéq-b.xmax=0
CA.VA-a.xmax=0 و CB.VBéq-b.xmax=0 
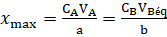
وبالتالي:
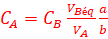
2. طرق المعايرة المباشرة :
1.2. المعايرة بقياس المواصلة – تطبيق :
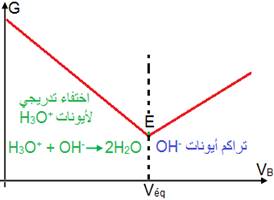
نتتبع تطور مواصلة جزء من محلول مائي لحمض الكلوريدريك, ذي تركيز مجهول CA بدلالة الحجم المضاف VB من محلول مائي للصودا, ذي تركيز CB معروف, فنحصل على المنحنى التالي:
انطلاقا من المنحنى نحصل على نقطة التكافؤ E , وبالتالي الحجم المضاف عند التكافؤ هو: Véq.
* لنحسب التركيز CA
حالة التفاعل
تقدم التفاعل
H3O+ + OH-
 2H2O
2H2O الحالة البدئية
x=0
وفير
ni(OH- )
ni(H3O+ )
أثناء التفاعل
x
وفير
ni(OH- )- x
ni(H3O+ )-x
الحالة النهائية
x=xmax
وفير
ni(OH- )- xmax
ni(H3O+ )-xmax
عند التكافؤ: ni(H3O+ )-xmax=0 و ni(OH- )- xmax=0
 CA.VA=xmax و CB.VBéq=xmax
CA.VA=xmax و CB.VBéq=xmaxوبالتالي:
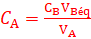
2.2. المعايرة الملوانية :
نعاير محلول كبريتات الحديد II , تركيزه مجهول C1, بواسطة محلول برمنغنات البوتاسيوم ذي تركيز معروف C2.
في البداية يختفي اللون البنفسجي بعد اختلاطه مع كبريتات الحديد II , حيث يتحول إلى أيونات المنغنيز Mn2+ عديمة اللون, وفق المعادلة التالية:
MnO4- + 5Fe2+ + 8H+
 Mn2+ + 5Fe3+ + 4H2O
Mn2+ + 5Fe3+ + 4H2O عند استهلاك كل أيونات Fe2+ لا تتفاعل أيونات MnO4- مما يفسر تلون الخليط.
* لنحسب التركيز المجهول C1
حالة التفاعل
تقدم التفاعل
MnO4- + 5Fe2++ 8H+
 Mn2+ + 5Fe3+ + 4H2O
Mn2+ + 5Fe3+ + 4H2Oالحالة البدئية
x=0
وفير
0
0
وفير
ni(Fe2+ )
ni(MnO4- )
أثناء التفاعل
x
وفير
5.x
x
وفير
ni(Fe2+ )-5.x
ni(MnO4- )- x
الحالة النهائية
x=xmax
وفير
5.xmax
xmax
وفير
ni(Fe2+ )-5.xmax
ni(MnO4- )- xmax
عند التكافؤ: ni(MnO4- )- xmax=0 و ni(Fe2+ )-5.xmax=0
 C1V1=5.xmax و
C2V2éq=xmax
C1V1=5.xmax و
C2V2éq=xmaxوبالتالي:
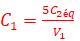
3. دقة المعايرة
تتعلق دقة المعايرة بدقة قياس كل معطى, C2, V1, V2éq.
مثلا :
* دقة C2: تتعلق بالطريقة المتبعة. لنعتبر C2m=0.030mol.L-1 , والدقة هي: ± 0.001 mol.L-1.
* دقة V1: تتعلق بدقة الماصة المعيارية. لنعتبر V1m=20.00mL , والدقة هي: ± 0.02mL .
* دقة V2éq: تتعلق بدقة السحاحة. لنعتبر V2éqm=13.30mL , والدقة هي: ± 0.05mL .
+ لنحسب مجال دقة التركيز C1
لدينا:
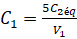
 C1m=0.10mol.L-1
C1m=0.10mol.L-1والدقة هي مجموع الدقات: ± 0.07mol.L-1
وبالتالي: 0.3 mol.L-1 ≤ C1≤ 0.17 mol.L-1