Les grandeurs liées aux quantités de matière
I. كمية المادة (تذكير)
المول هو كمية المادة لمجموعة تحتوي على عدد من المكونات الأساسية يساوي عدد الذرات الموجودة في 12g من الكربون 12. وهو 6 ,02 10 23 ذرة. ويطلق عليه اسم عدد أفوكادرو . ورمزه هو N A .
بالنسبة لعينة تحتوي على عدد N من المكونات الأساسية, تكون كمية مادة هذه العينة هي n .
![]() حيث:
حيث:
![]() (mol)
(mol)
![]() (mol
-1
)
(mol
-1
)
II. كمية المادة بالنسبة للأجسام الصلبة والسائلة
1. كمية المادة والكتلة
![]() كمية المادة
n
لعينة كتلتها
m
مكونة من نوع كيميائي
X
كتلته المولية
M(X)
هي:
(g)
كمية المادة
n
لعينة كتلتها
m
مكونة من نوع كيميائي
X
كتلته المولية
M(X)
هي:
(g)
![]()
![]() (mol)
(mol)
![]()
(g.mol -1 )
تمرين تطبيقي:
نقيس كتلة m 1 = 100 g من الماء الخالص و أيضا كتلة m 2 = 100 g من الحديد.
1. احسب كمية مادة جزيئات الماء الموجودة في الكتلة m 1 .
2. احسب كمية مادة ذرات الحديد الموجودة في الكتلة m 2 .
2. كمية المادة والحجم
a.
![]() الكتلة الحجمية والكثافة
(g)
الكتلة الحجمية والكثافة
(g)
ü
![]()
![]() الكتلة الحجمية يعبر عنها بالعلاقة:
الكتلة الحجمية يعبر عنها بالعلاقة:
![]() (g.m
-3
)
(g.m
-3
)
(m -3 )
ü
كثافة جسم ما, ذي كتلة حجمية
![]() بالنسبة لجسم مرجعي ذي كتلة حجمية
بالنسبة لجسم مرجعي ذي كتلة حجمية
![]() هي:
هي:
![]() ليس لها وحدة.
ليس لها وحدة.
ملحوظة:
بالنسبة للأجسام الصلبة والسائلة يتم اختيار الماء كجسم مرجعي.
![]() .
.
b. علاقة كمية المادة بالحجم
كمية مادة
n
لعينة حجمها
V
وكتلتها الحجمية
![]() تحسب بالعلاقة:
تحسب بالعلاقة:
![]()
تمرين تطبيقي:
الهيكسان
C
6
H
14
جسم سائل عند درجة حرارة
20°C
, كتلته الحجمية
![]() .
.
احسب الحجم V للهيكسان الذي يجب قياسه بواسطة مخبار مدرج للحصول على n = 0,1 mol من هذا السائل.
III. كمية المادة بالنسبة للأجسام الغازية
1. علاقة كمية مادة غاز بحجم العينة (تذكير)
ü الحجم المولي V m لغاز هو الحجم الذي يحتله مول واحد من الغاز في ظروف معينة لدرجة الحرارة والضغط. وحدته هي : L.mol -1 .
ü
![]() كمية مادة عينة من غاز حجمها
V
هي:
(L)
كمية مادة عينة من غاز حجمها
V
هي:
(L)
![]()
![]()
![]() (mol)
(mol)
(L.mol -1 )
ملحوظة: في الشروط النظامية (t 0 = 0°C ; p 0 = 1 atm) V 0 = 22,4 L.mol -1
2. قانون بويل-ماريوط
نص القانون: عند درجة حرارة ثابتة, وبالنسبة لكمية معينة من غاز يبقى الجداء p.V ثابتا.
3.
 السلم المطلق لدرجة الحرارة
السلم المطلق لدرجة الحرارة
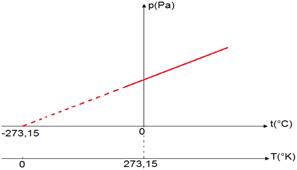
نأخذ كمية معينة من غاز حيث يبقى حجمه ثابتا, وندرس تغير الضغط p بدلالة الدرجة الحرارة t .
مكنت النتائج التجريبية من خط المنحنى p = f(t) .
يتقاطع المنحنى مع المحور الأفقي عند درجة حرارة -273,15°C وهي حد أدنى مطلق لدرجة الحرارة لا يمكن وجود ما هو أصغر منه.
نزيح محور الاراتيب إلى النقطة -273,15 °C فنحصل على ما يسمى بالتدريج المطلق. فعوض محور درجات الحرارة المئوية (°C) نستعمل محور درجات الحرارة المطلقة. T . المعبر عنها بالوحدة K (Kelvin) .
![]() إذن العلاقة بين درجة الحرارة المئوية و المطلقة هي:
(°C)
إذن العلاقة بين درجة الحرارة المئوية و المطلقة هي:
(°C)
![]() T = t + 273,15
(°K)
T = t + 273,15
(°K)
ملحوظة: درجة الحرارة المئوية t = -273,15 °C توافق T = 0 °K و تسمى الصفر المطلق .
4. الغاز الكامل
a. نموذج الغاز الكامل
يعتبر الغاز كاملا إذا كان:
ü جزيئاته عبارة عن كريات متناثرة.
ü لا تؤثر جزيئاته على بعضها البعض عن بعد.
ü التصادمات بين جزيئات الغاز كلها مرنة.
ملحوظة:
ü يخضع الغاز الكامل خضوعا تاما لقانون بويل-ماريوط.
ü تتصرف الغازات الحقيقية, تحت ضغط ضعيف كغاز كامل.
b. معادلة الحالة للغاز الكامل
تتميز حالة غاز بأربع متغيرات وهي الضغط p , و الحجم V , ودرجة الحرارة T , وكمية المادة n , وهي تسمى متغيرات الحالة .
بينت التجارب أن متغيرات الحالة لغاز كامل مرتبطة فيما بينها بالعلاقة: p.V = n.R.T معادلة الحالة للغازات الكاملة .
حيث R : ثابتة الغازات الكاملة . قيمتها:
ü R=8,314Pa.m 3 .K -1 .mol -1 عندما يعبر عن: V(m 3 ) ; T(°K) ; n(mol) ; p(Pa)
ü R = 0,082 atm.L.K -1 .mol -1 عندما يعبر عن: V(L) T(°K) ; n(mol) ; p(atm)
تمرين تطبيقي:
احسب كمية مادة الهواء داخل حوجلة حجمها V = 0,5 L في الظروف الاعتيادية لدرجة الحرارة والضغط (p = 1,013 10 5 Pa ; t = 20 °C) .