التحولات السريعة و التحولات البطيئة
-
1. Rappel sur couples réducteur / oxydant:
-
1.1. Oxydant :
Un oxydant est un espèce chimique capable d'acquérir (gagner) un ou plusieurs électrons lors d'une réaction chimique..
-
1.2. réducteur :
Le réducteur est un espèce chimique capable de perdre un ou plusieurs électrons au cours d'une réaction chimique.
-
1.3. Réaction d'oxydoréduction :
Réaction d'oxydoréduction dans laquelle des électrons sont échangés entre deux réactions: l'agent réducteur et l'oxydant.
-
1.4. Exemple :
Nous mettons une plaque de zinc dans un bécher contenant une solution de sulfate de cuivre II (Cu2+aq+SO42-aq) pendant une longue période et remarquons la disparition de la couleur bleue et la formation de cuivre métallique
couples demi-équation Cu2+aq/Cu Cu 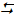 Cu2+aq +2e-
Cu2+aq +2e-
Zn2+aq/Zn Zn2+aq + 2e- 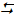 Zn
Zn
L'équation chimique résultante Zn2+aq + Cu 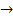 Cu2+aq +Zn
Cu2+aq +Zn
-
-
2. Transformations rapides et transitions lentes:
-
2.1. Transformations rapides :
Une transformation chimique rapide est une transformation qui se produisent en peu de temps (en une durée trop courte), donc on ne peut pas suivre l'évolution par les yeux ou avec les appareils de mesure habituels.
-
2.2. Transformation lentes :
Une transformation chimique lente est une transformation qui se produisent en quelques minutes ou plusieurs heures, donc peuvent être suivies à l'œil nu ou avec un instrument de mesure.
-
-
3. Facteurs cinétiques:
-
3.1. Définition d'un facteur cinétique :
Nous appelons un facteur cinétique, chaque paramètre ou grandeur qui peut modifier l'évolution d'un groupe chimique.
-
3.2. Effet de la température :
Plus la température est élevée, plus le système chimique évoluera rapidement
-
3.3. Effet des concentrations de réactif :
Plus la concentration des réactifs est élevée, plus le système chimique évoluera rapidement
-