Transformations chimiques s'effectuant dans les deux sens
-
1. التفاعلات حمض- قاعدة : (تذكير) :
-
1.1. تعاريف
الحمض : حسب برونشتد ، هو كل نوع كيميائي قادر على فقدان بروتون H+ خلال تفاعل كيميائي . القاعدة : حسب برونشتد ، هي كل نوع كيميائي قادر على اكتساب بروتون H+ خلال تفاعل كيميائي .
المزدوجة قاعدة/حمض : HA/A- : تتكون المزدوجة قاعدة/حمض من حمض A وقاعدته المقترنة A -. نصف المعادلة : نربط المزدوجة قاعدة/حمض بنصف معادلة تمثل الانتقال من حمض إلى قاعدته المرافقة (أو العكس) بفقدان (أو كسب) أيون الهيدروجين H+
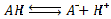
-
2.1. التفاعل حمض قاعدة
هو تبادل لبروتون H+ بين الحمض HA1 و القاعدةA2-.
* ذوبان كلورور الهيدروجين في الماء . : H2O + HCl → H3O++Cl- المزدوجتان هما : HCl/Cl- : و H3O+/H2O :
-
-
2. تعريف و قياس pH محلول مائي :
-
1.2. تعريف: " يعرف pH محلول مائي مخفف بالعلاقة:
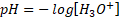 هذه العلاقة مكافئة ل :
هذه العلاقة مكافئة ل : 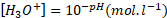 ".
".
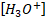 : تركيز أيونات الأوكسونيوم في المحلول ب mol.L-1.
: تركيز أيونات الأوكسونيوم في المحلول ب mol.L-1. -
2.2. قياس pH محلول مائي :
بواسطة كواشف ملونة بواسطة ورق pH بواسطة pH-متر.  مواد عضوية يتغير لونها حسب قيمة pH المحلول
مواد عضوية يتغير لونها حسب قيمة pH المحلول
 ورق خاص يتغير لونه بعد تبليله بالمحلول ، و نقارن لونه مع سلم الألوان المرجعية مصحوب بقيم pH الموافق لكل لون
ورق خاص يتغير لونه بعد تبليله بالمحلول ، و نقارن لونه مع سلم الألوان المرجعية مصحوب بقيم pH الموافق لكل لون
 جهاز يمكن من قياس مباشر ل pH محلول بدقة من. و يتكون من الكترود حساس للايونات H3O+ مرتبط بفولطمتر رقمي مدرج بوحدة pH
جهاز يمكن من قياس مباشر ل pH محلول بدقة من. و يتكون من الكترود حساس للايونات H3O+ مرتبط بفولطمتر رقمي مدرج بوحدة pH
-
3. التحولات الكلية و غير الكلية :
-
1.3. نسبة التقدم النهائي – Taux d’avancement:
" نسبة التقدم النهائي لتفاعل كيميائي هو خارج قسمة التقدم النهائي
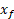 لتفاعل على تقدمه الأقصى
لتفاعل على تقدمه الأقصى 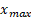 " :
" : 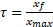
-
1.3. التحولات الكلية و غير الكلية:
* التحولات الكلية (التامة) : نقول إن التحول يكون كاملاً عندما ينتهي باختفاء أحد المتفاعلات (المتفاعل المحدد) و عنده تتحقق العلاقة xf=xm و بالتالي τ=1 اي τ=100% المتفاعل المحد تفاعل كليا
* التحولات غير الكلية (المحدودة) : نقول ان التحول غير كلي عندما يصل الى نهايته مع عدم اختفاء المتفاعلات كليا و عنده تتحقق العلاقة xf<xm و بالتالي τ<1 اي τ<100% المتفاعل المحد لم يتفاعل كليا
-
-
4. حالة توازن مجموعة كيميائية :
-
- التفسير الميكروسكوبي لحالة التوازن الديناميكي: ( خاص بالعلوم الرياضية (أ و ب) و العلوم الفيزيائية ):
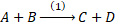
تتناقص كميتي A و B ، و بالتالي يتناقص عدد التصادمات الفعالة بينهما مما يؤدي إلى تناقص السرعة
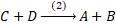
تتزايد كميتي C و D و بالتالي يزداد عدد التصادمات بينهما مما يؤدي إلى تزايد السرعة للتفاعل في المنحى العكسي (2).
عندما تتساوى السرعتان v1 و v2 ، فإن كمية المتفاعل A مثلا ، التي تٌستهلك في التفاعل المباشر (1) تساوي كميته المتكونة خلال التفاعل في المنحى العكسي (2) ، و هكذا تبقى التراكيز المولية للمجموعة ثابتة خلال الزمن .
"في حالة توازن مجموعة كيميائية ، يكون في كل لحظة عدد الدقائق المختفية بالتفاعل في المنحى المباشر ، مساويا لعدد الدقائق المتكونة بالتفاعل في المنحى العكسي ".
-