Décroissance radioactive
-
1. النوى و النظائر :
-
1.1. تركيب النواة
رمز العنصر الكيميائي : X
رمز النواة :
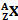
عدد البروتونات (عدد الشحنة) : Z
عدد النوترونات : N=A-Z
عدد النويات (عدد الكتلة) : A
مثال :
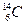 : A=14 ; Z=6 ; N=8
: A=14 ; Z=6 ; N=8
-
2.1. النويدات - Les nucléides
النويدة : هي مجموعة النوى التي تتميز بعدد معين من البرتونات Z و من النوترونات ، و رمزها
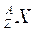 .
.أمثلة:
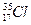 : نويدة لعنصر الكلور
: نويدة لعنصر الكلور
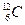 و
و 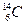 : نويدتان لعنصر الكربون
: نويدتان لعنصر الكربون -
3.1. النظائر - Isotopes :
" نظائر العنصر الكيميائي هي لها نفس عدد الشحنة
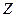 تختلف في عدد الكتلة
تختلف في عدد الكتلة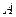 ."
."أمثلة:
*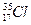 و
و 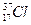
*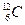 و
و 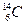
*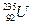 و
و 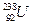 .
." الوفارة L’abandance "
تمثل العلاقة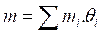 كتلة خليط من نظائر عنصر ما .
كتلة خليط من نظائر عنصر ما .
*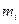 : كتلة النظير
: كتلة النظير 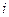 .
.
*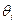 : وفارة النظير
: وفارة النظير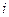 و يعبر عنها بالنسبة المؤوية.
و يعبر عنها بالنسبة المؤوية.
-
-
2. التحولات النووية التلقائية – النشاط الإشعاعي:
-
1.2. النشاط الإشعاعي :
تحول طبيعي ، و غير مرتقب في الزمن ، تتحول خلاله نواة غير مستقرة إلى نواة أخرى اكتر استقرارا و إلى حالة إثارة أقل طاقة
* نسمي نواة مستقرة ،كل نواة تحتفظ بصفة دائمة بنفس التركيب.
* نسمي نواة مشعة ≡ نواة غير مستقرة ، كل نواة تتحول تلقائيا إلى نواة أخرى بعد بعثها إشعاعات.
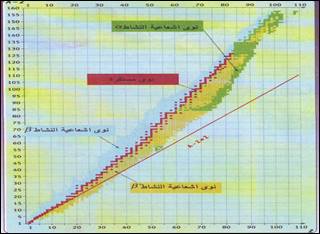
* يمثل الشكل المقابل مخطط (N ;Z) ، وهو مخطط يحدد موقع النوى المستقرة و النوى المشعة، حيث تُمَثَّلُ كل نواة بمربع صغير أفصوله Z عدد بروتونات النواة ، و أرتوبه N عدد نوتروناتها.
* منطقة الاستقرار تضم النوى المستقرة :
++ في المجال Z<20 : النوى الخفيفة المستقرة تحقق العلاقة A=2Z او N=Z تقريبا
++ في المجال Z>20 : منطقة الاستقرار فوق المستقيم ذي المعادلة N=Z
++ في المجال Z>70 : النوى الثقيلة المستقرة تحقق تقريبا A=2,5Z -
2.2. الأنشطة الإشعاعية :
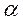 و
و 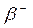 و
و 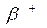 و
و 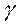
نوع النشاط * النشاط الإشعاعي 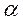
* النشاط الإشعاعي 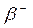
* النشاط الإشعاعي 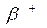
* النشاط الإشعاعي 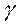
قانون الانحفاظ قانون سودي خلال تحول نووي تنحفظ الشحنة الكهربائية
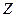 و كذلك العدد الإجمالي للنويات
و كذلك العدد الإجمالي للنويات 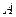 .
.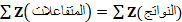 و
و 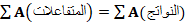
تعريف تفتت نووي طبيعي و تلقائي تنبعث خلاله الدقيقة
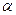
الهيليوم
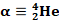
تفتت نووي طبيعي و تلقائي تنبعث خلاله الدقيقة
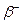
الكترون
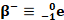
تفتت نووي طبيعي و تلقائي تنبعث خلاله الدقيقة
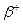
بوزترون
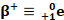
غالبا ما يرافق الاشعاعات السابقة ناتجا عن فقدان النويدة المتولدة لإثارتها ، : موجات كهرمغنطيسية
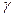 ، ذات طاقة كبيرة جدا
، ذات طاقة كبيرة جدامعادلة التحول 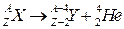
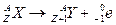
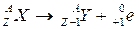
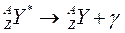
الميكانيزم تفقد النواة بروتونيين و نوترونيين تحول نوترون إلى بروتون داخل النواة حسب المعادلة التالية:
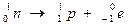
بعد تحول بروتون إلى نوترون داخل النواة حسب المعادلة التالية:
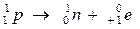
تفقد النواة الطاقة امثلة 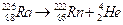
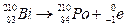
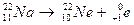
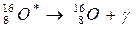
-
-
3. التناقص الإشعاعي:
-
1.3. الصبغة العشوائية للنشاط الإشعاعي :
النشاط الإشعاعي ظاهرة عشوائية تحدث تلقائيا ، إذن لا يمكن التنبؤ باللحظة التي يحدث فيها التفتت و لا يمكن تغيير خاصيات هذه الظاهرة .
-
2.3. قانون التناقص الإشعاعي:
قانون التناقص الإشعاعي :
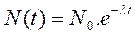
* λ تمثل تابتة التفتت
* N(t) : عدد النوى المتبقية في العينة التي لم تتفتت بعد في اللحظة t.
* N0 عدد نويدة مشعة في اللحظة t=0 : أي البدئية
-
3.3. ثابتة الزمن- عمر النصف :
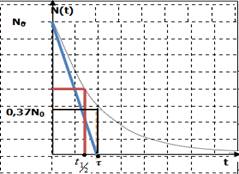
* ثابتة الزمن
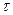 : /p>
: /p>تعرف
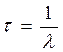
* عمر النصف :
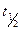
نسمي عمر النصف
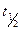 المدة الزمنية اللازمة لتفتت نصف عدد نوى عينة.
المدة الزمنية اللازمة لتفتت نصف عدد نوى عينة.* العلاقة بين t1/2 و λ
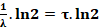
-
4.3. نشاط عينة مشعة :
نشاط عينة مشعة : هو عدد في وحدة الزمن :
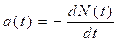 مع
مع 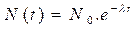
و بالتالي :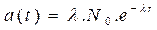
وحدة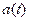 في (SI) هي : Bq (Becquerel).
في (SI) هي : Bq (Becquerel).
و يستعمل كذلك الكوري Curie :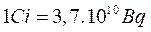
نضع :
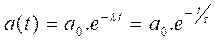 مع
مع 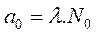

ملحوظة: يقاس النشاط الاشعاعي بواسطة عدادات مثل عداد "Geiger"
-
-
4. التأريخ بالنشاط الإشعاعي :
-
التأريخ بالكربربون (14) مثلا :
* في الجو تبقى نسبة الكربون 14 تابثة و بالتغذية و التنفس يتبادل الكائن الحي الكربون مع الوسط الخارجي و هذا يجعل نسبة الكربون 14 فيه تابثة
* عند تموت الكائنات الحية يتوقف التبادل فتتناقص نسبة الكربون
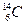 من ، بسبب تفتت نوى
من ، بسبب تفتت نوى 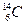 حسب المعادلة التالية :
حسب المعادلة التالية : 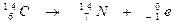
نعتبر توقف التبادل الكربون مع الوسط الخارجي (موت الكائن الحي) اصلا للتواريخ t=0
نأخد كمية كتلتها m من العنصر المراد تحديد عمره (ميت) و فنحدد نشاطها a(t)
نأخد نفس الكمية ذات الكتلة m من العنصر الحي فنحدد نشاطها a0 ويوافق نشاط الميت عندما كان حيا
و بتطبيق قانون التناقص
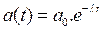 نجد :
نجد :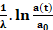
و بالتالي المدة الزمنية الفاصلة بين تاريخ الوفاة (t0=0) و تاريخ اجراء التأريخ t هو : Δt =t-t0=t
ملحوظة: تستعمل هذه الطريقة لتحديد تاريخ عينات لا يزيد عمرها عن 40000 سنة .
( لأن العينات الأطول عمرا تحتوي على كمية ضئيلة جدا من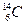 )
)
-