Etat d’équilibre d’un système chimique
-
1. خارج التفاعل Quotient de réaction – Qr – :
نعتبر مجموعة كيميائية بإمكانها الخضوع لتحول كيميائي منمذج
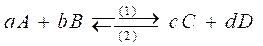
* A و B و C و D : أنواع كيميائية مذابة في محلول مائي.
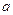 و
و 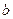 و
و 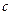 و
و 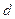 : المعاملات
: المعاملاتيعرف خارج التفاعل المقرون بالتفاعل في المنحى المباشر (1) بالنسبة لحالة معينة للمجموعة الكيميائية بالعلاقة :
استثناءات :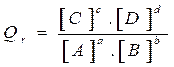
في حالة الماء مذيب و الاجسام الصلبة يعوض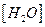 و تركيز جسم صلب بالعدد 1
و تركيز جسم صلب بالعدد 1
امثلة :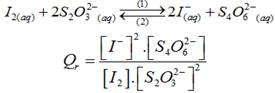
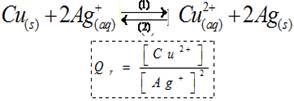
-
2. خارج التفاعل عند التوازن:
-
1.2. تعريف :
" نعتبر التفاعل
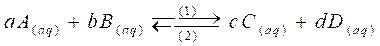
نسمي خارج التفاعل عند التوازن
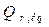 ، القيمة التي يأخذها خارج التفاعل عند تكون المجموعة المدروسة في حالة التوازن".
، القيمة التي يأخذها خارج التفاعل عند تكون المجموعة المدروسة في حالة التوازن".خارج التفاعل عند التوازن :
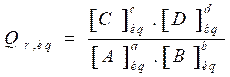
-
2.2. تحديد
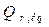 بواسطة المواصلة :
بواسطة المواصلة :خارج التفاعل عند التوازن لتفاعل حمض الايثانويك مع الماء هو : Qr,éq=1,58.10-5 (انظر تصحيح التمرين)
-
-
3. ثابتة التوازن المقرونة بتحول كيميائي:
-
1.3. تأثير الحالة البدئية على خارج التفاعل في حالة التوازن :
في نفس درجة الحرارة يبقى خارج التفاعل في حالة التوازن تابثا و لا يتعلق بتركيب الحالة البدئية
-
2.3. تعريف ثابتة :
" نقرن بكل معادلة تفاعل ثابتة تسمى ثابتة ، يرمز لها بالحرف K . في حالة التوازن
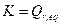 .
.K : ثابتة لا تتعلق إلا بدرجة الحرارة. ( K بدون وحدة )
-
-
4. نسبة التقدم النهائي في حالة التوازن :
-
1.4. تأثير الحالة البدئية على نسبة التقدم النهائي :
خارج التفاعل في حالة التوازن.
بتغير التركيز البدئي للمتفاعلات (التركيب البدئي للمجموعة ) فان نسبة تقدم النهائي تتغير.
-
2.4. تأثير ثابتة التوازن على نسبة التقدم النهائي :
كلما كانت ثابتة التوازن كبيرة كلما كان كانت نسبة التقدم النهائي
ملحوظة :عند K>104 فان τ=99% بالتالي يمكن اعتبار التحول كلي
-