Transformations associées aux réactions acide-base en solution aqueuse
-
1. الجداء الأيوني للماء :
-
1.1. التحليل البروتوني الذاتي للماء
- للماء الخالص عند 25oC موصلية
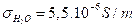 و pH=7,0 موصلية غير منعدمة و هذا يدل على وجود ايونات بالماء
و pH=7,0 موصلية غير منعدمة و هذا يدل على وجود ايونات بالماء- الماء H2O قاعدة للمزدوجة H3O+(aq)/H2O(ℓ)، و حمض للمزدوجة H2O(ℓ)/OH-(aq).
- معادلة التفاعل بين الحمض H2O و القاعدةH2O هو :
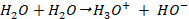 و تسمى معادلة التحلل البرتوني الذاتي للماء و هو تحول جد محدود .
و تسمى معادلة التحلل البرتوني الذاتي للماء و هو تحول جد محدود .
- نسمي تابثة التوازن المقرون بمعادلة التحلل البروتوني الذاتي للماء بالجداء الأيوني للماء تعبيره : Ke=[H3O+].[OH-]
مثال:
800C 600C 250C درجة الحرارة 2,5.10-13 1,0.10-13 1,0.10-14 قيمة Ke * يمكن كذلك تعريف مقدار آخر
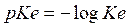
-
2.1. المحاليل المحايدة و الحمضية و القاعدية :
المحاليل الحمضية المحاليل المحايدة المحاليل القاعدية [H3O+]>[OH-] [H3O+].[H3O+]>[OH-].[H3O+] [H3O+]2>Ke pH<Ke/2 [H3O+]=[OH-] [H3O+].[H3O+]=[OH-].[H3O+] [H3O+]2=Ke pH=Ke/2 [H3O+]<[OH-] [H3O+].[H3O+]<[OH-].[H3O+] [H3O+]2<Ke pH>Ke/2 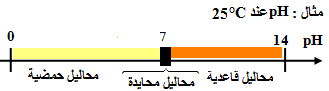
-
-
2. ثابتة الحمضية لمزدوجة حمض قاعدة :
-
1.2. تعريف :
تكتب معادلة التفاعل الذي يحدث عند ذوبان حمض AH في الماء كالتالي : AH(aq)+H2O(l)↔A-(aq)+H3O+(aq)
* نسمي ثابتة التوازن المقرونة بهذا التفاعل ، ثابتة الحمضية نرمز لها بـ KA و نعبر عنها ب:
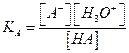
* نعرف الثابتة pKA للمزدوجة HA/A- بالعلاقة :
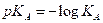
أمثلة عند 250C
المزدوجة KA pKA 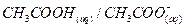
1,58.10-5 4,8 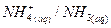
6,3.10-10 9,2 ملحوظة: KA لا تتعلق إلا بدرجة الحرارة و بطبيعة الحمض
-
2.2. العلاقة بين pH و ثابتة الحمضية KA (و pKA) :
بالنسبة لمزدوجة A/B نكتب :
.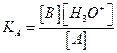
العلاقة بين pH و pKA:
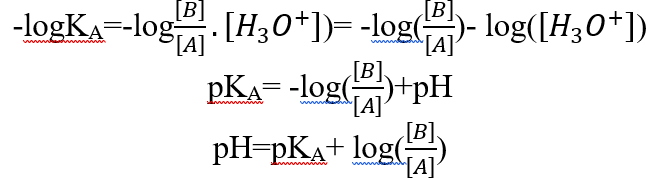
-
2.3. ثابتة التوازن المقرونة بتفاعل حمض – قاعدة :
نعتبر التفاعل حمض-قاعدة بين المزدوجتين
AH(aq)/A-(aq) ذات تابثة الحمضية
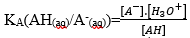
و BH(aq)/B-(aq) ذات تابثة الحمضية
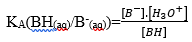
معادلة التفاعل : AH(aq)+B-(aq) ↔ A-(aq)+BH(aq)
تعبير تابثة التوازن :
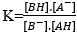
تعبير K بدلالة K(AH(aq)/A-(aq)) و K(BH(aq)/B-(aq))
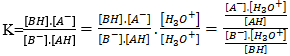
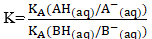 اي
اي 
-
-
3. مقارنة سلوك الأحماض في محلول مائي :
-
1.3. مقارنة سلوك الأحماض في محلول مائي :
بتفاعل الحمض مع الماء فأن تابثة التوازن هي تابثة الحمضية
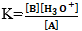 مع
مع 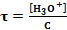
نجد
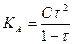
منه نستنتج انه بالنسبة لتركيز نفسه يكون حمض أقوى (τ كبيرة ) كلما كانت تابثة الحمضية KA كبيرة اي كلما كانتpKA اصغر
-
2.3. مقارنة سلوك القواعد في محلول مائي :
بتفاعل القاعدة مع الماء فان
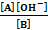 مع
مع 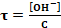 نجد
نجد 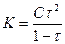
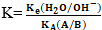 ومنه
ومنه 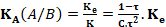
نستنتج انه بالنسبة لتركيز نفسه تكون قاعدة أقوى (τ كبيرة ) ، كلما كانت KA صغيرة اي كلما كانت pKA اكبر.
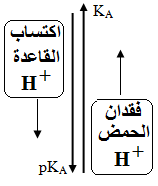
-
-
4. مخطط الهيمنة و التوزيع :
-
1.4. مخطط الهيمنة :
بالنسبة لمزدوجة A(aq)/B(aq) في محلول مائي ، تتحقق العلاقة:
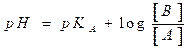 أي
أي 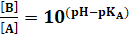
- إذا كان
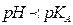 : اي
: اي 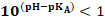 و التالي :
و التالي : 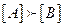 : الحمض مهيمن في الوسط.
: الحمض مهيمن في الوسط.- إذا كان
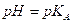 : اي
: اي 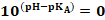 و التالي :
و التالي : 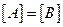 : تساوي هيمنة الحمض و القاعدة
: تساوي هيمنة الحمض و القاعدة- إذا كان
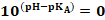 : اي
: اي 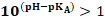 و التالي :
و التالي : 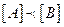 : القاعدة مهيمنة في الوسط.
: القاعدة مهيمنة في الوسط.
-
2.4. مخطط التوزيع :
لنعتبر محلولا مائيا ، يحتوي على الحمض A و قاعدته المرافقة B .
* نسمي نسبة الحمض في
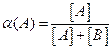
* نسمي نسبة القاعدة في محلول:
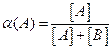
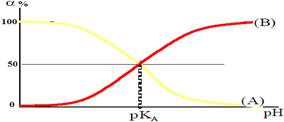
* يمثل المخطط المقابل ، مخطط التوزيع لنوعي المزدوجة A/B ، تطور نسبة للحمض و القاعدة بدلالة pH المحلول ، عند نفس درجة
* عند تقاطع المنحنيين ، يكون
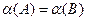 و منه :
و منه : 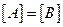 أي أن :
أي أن : 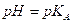 .
. -
2.4. حالة الكواشف الملونة :
* تعريف: الكاشف الملون حمضي-قاعدي ، مزدوجة حمضية-قاعدية، نرمز لها ب HInd/Ind- ، بحيث يكون للشكلين الحمضي HInd و القاعدي Ind- لونان مختلفان في محلول مائي.
* ثابتة الحمضية لكاشف ملون : نرمز لها بـ KA,Ind و نعبر عنها بـ
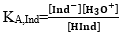
* مجال هيمنة لون الحمض و لون القاعدة
* نقبل ان لون الحمض يغلب في الوسط إذا كان تركيز الحمض HInd اكبر بعشر مرات من تركيز القاعدةInd-
أي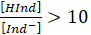 مع
مع 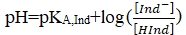
و بالتالي نجد pH<pKA,Ind -1* نقبل ان لون القاعدة يغلب في الوسط إذا كان تركيز القاعدة Ind- اكبر بعشر مرات من تركيز الحمض HInd
أي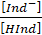 مع
مع 
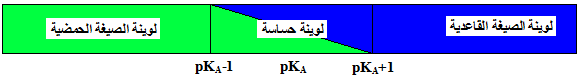
و بالتالي نجد pH>pKA,Ind+1* منطقة انعطاف الكاشف الملون : هي المنطقة التي يغير فيها الكاشف الملون لونه من لون الصيغة القاعدية الى لون الصيغة الحمضية او العكس
pKA,Ind-1<pH<pKA,Ind +1
في هذه الحالة يأخذ الكاشف الملون لون وسطيا بين لوني الحمض و القاعدة يسمى لوينة حساسة- teinte sensible
* بعض الكواشف الملونة ومميزاتها :
الكاشف الملون لون الشكل القاعدي منطقة الانعطاف لون الشكل الحمضي الهيليانتين أصفــر 3,1 <-> 4,4 أحمــر أخضر البروموكريزول أزرق 3,8 <-> 5,4 أصفــر أحمر الكلوروفينول أحمــر 4,8 <-> 6,4 أصفــر
-
-
5. المعايرة حمض-قاعدة :
-
1.5. المعايرة حمض-قاعدة بقياس pH :
* مبدأ المعايرة
تهدف المعاير ة الى تحديد تركيز محلول مجهول و ذالك بانجاز تفاعل حمض – قاعدة يسمى تفاعل المعايرة و يجب ان يكون سريعا و كليا و انتقائيا* التركيب التجريبي
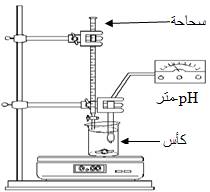
* التكافؤ الحمضي – القاعدي عند التكافؤ يكون الخليط متناسبا و تستهلك المتفاعلات وفق المعاملات التناسبية
ونكتب
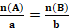
حيث : a و b معاملات تناسبية .في كل تحول حمضي قاعدي a=b=1
علاقة التكافؤ الحمضي القاعدي n(A)=n(B)
اي : CA.VA=CB.VB* تحديد نقطة التكافؤ.
طريقة المماسات
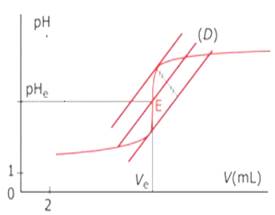
نخط المماسين T1 و T2 للمنحنى pH=f(VB) في النقطتين A و B ، ثم نخط المستقيم (D) الموازي ل T1 و T2 الموجود على نفس المسافة بينهما نقطة تقاطع مع المنحنى pH=f(V) تسمي E.
طريقة الدالة المشتقة
نرسم المنحنيين pH=f(VB) ، و
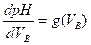 حيث يمثل الدالة المشتقة ل pH
بدلالة الحجم V عند نقطة التكافؤ تأخد الدالة
حيث يمثل الدالة المشتقة ل pH
بدلالة الحجم V عند نقطة التكافؤ تأخد الدالة
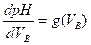
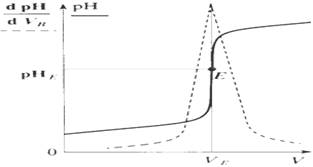
قيمة قصوى : في حالة معايرة الحمض بالقاعدة
او قيمة دنيا : في حالة معايرة القاعدة بالحمض
-
2.5. المعايرة الملوانية حمض-قاعدة :
هي معايرة حمضية –قاعدية حيث نمعلم معلمة التكافؤ بتغير لون الوسط و ذلك باستعمال كاشف ملون مناسب
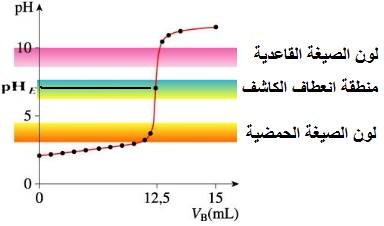
يكون الكاشف الملون صالحا لتحديد التكافؤ خلال معايرة حمضية قاعدية إذا كانت منطقة انعطافه تضم قيمة pHE المحلول عند التكافؤ
-