التناقص الاشعاعي
-
1. introduction::
-
1.1. Composition du noyau
Symbole de l'élément chimique: X
Symbole du noyau :
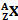
Nombre de protons (nombre de charge) : Z
Le nombre de neutrons : N=A-Z
Nombre de masse (nombre de nucléons) : A
Exemple :
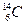 : A=14 ; Z=6 ; N=8
: A=14 ; Z=6 ; N=8 -
2.1. Les nucléides :
Nuclide: C'est un groupe de noyaux caractérisé par un certain nombre de protons et neutrons Z, et leur symbole
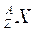 .
. Exemples:
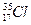 : un nucléide du chlore
: un nucléide du chlore 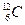 et
et 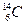 : Deux nucléides de carbone
: Deux nucléides de carbone -
3.1. Isotopes :
" Les isotopes de l'élément chimique ont le même nombre de charge Z mais ils diffèrent par le nombre de masse A."
Exemples: *
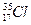 et
et 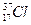 *
* 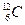 et
et 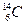 *
* 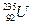 et
et 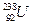 .
. " L’abandance " La relation
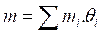 représente La masse d'un mélange d'isotopes d'un élément . *
représente La masse d'un mélange d'isotopes d'un élément . * 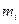 : Masse de l'isotope
: Masse de l'isotope 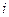 . *
. * 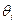 : L’abandance de l'isotope
: L’abandance de l'isotope 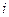 Et elle est exprimée en pourcentage .
Et elle est exprimée en pourcentage .
-
-
2. Transformations nucléaires spontanées et la Radioactivité:
-
1.2. la Radioactivité :
Une transformation naturelle , inattendue dans le temps , Au cours de laquelle un noyau instable se transforme en un autre noyau plus stable , ou bien dans un état moins exité
* Nous appelons un noyau stable, chaque noyau conservant toujours la même structure.
* Nous appelons un noyau radioactif un noyau instable, chaque noyau qui se transforme automatiquement en un autre noyau après avoir émis un rayonnement.
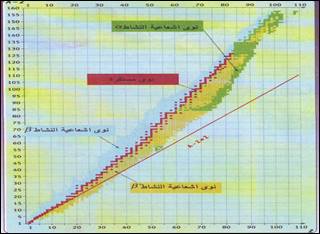
* La figure ci-contre est un graphique (N; Z), qui est un diagramme qui localise les noyaux stables et les noyaux rayonnants, où chaque noyau est représenté par un petit carré dont son Abscisse est Nombre Z de protons du noyau, Et son ordonnée est N le nombre de ses neutrons.
* La zone de stabilité comprend les noyaux stables: ++ Dans l'intervalle Z<20 : Noyaux stables légers ; La relation A = 2Z ou N = Z est approximativement atteinte ++ Dans l'intervalle Z>20 : La région de stabilité est au-dessus de la droite d'équation N = Z ++ Dans l'intervalle Z>70 : Noyaux lourds stables vérifient grossièrement A = 2,5Z
-
2.2. Les rayonnements (ou Radioactivités) :
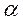 et
et 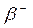 et
et 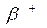 et
et 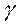
Type de la radioactivité * La radioactivité alpha : 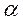
* La radioactivité bêta moins 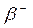
* La radioactivité bêta plus 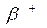
* La radioactivité gama 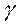
La loi de conservation est la loi de Soddy Lors d'une transformation nucléaire, il y a conservation de la charge électrique Z et du nombre de masse A. .
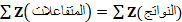 et
et 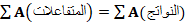
Définition désintégration nucléaire naturelle et spontanée pendant laquelle la particule émise est
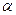
Hélium
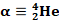
désintégration nucléaire naturelle et spontanée pendant laquelle la particule émise est
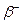
Électron
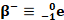
désintégration nucléaire naturelle et spontanée pendant laquelle la particule émise est
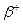
Positron
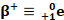
Souvent les radiations antérieures sont accompagnées par des ondes électromagnétiques
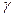 de très haute énergie , et qui sont provoqués par la perte de l'excitation de le nucléide généré
de très haute énergie , et qui sont provoqués par la perte de l'excitation de le nucléide généré Équation de transformation nucléaire 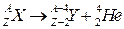
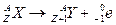
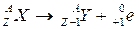
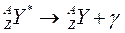
Mécanisme Le noyau perd les protoniens et les neutrons La transformation d'un neutron en proton à l'intérieur du noyau selon l'équation suivante: 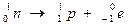
La transformation d'un proton en neutron à l'intérieur du noyau selon l'équation suivante: 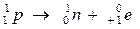
Le noyau perd de l'énergie Exemples 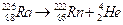
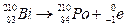
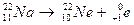
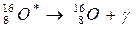
-
-
3. Décroissance radioactive:
-
1.3. Caractère aléatoire de la radioactivité :
La radioactivité est un phénomène aléatoire qui se produit spontanément, de sorte que le moment auquel la desintegration se produira ne peut pas être prédit et Les propriétés de ce phénomène ne peuvent pas être modifiées .
-
2.3. Loi de décroissance radioactive:
Loi de décroissance radioactive :
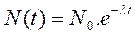
* λ Représente la constante de desintegration
* N(t) : Le nombre de noyaux restant dans l'échantillon qui ne s'est pas encore désintégré au moment t.
* N0 Le nombre de radionucléides à l'instant t = 0: c'est-à-dire Le nombre initiale
-
3.3. Constante de temps et la demi-vie :
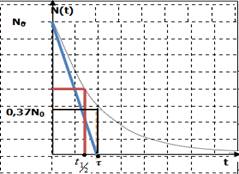
* Constante de temps
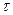 :
: définir par la relation
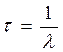
* la demi-vie :
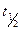
Nous appelons la demi-vie
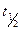 le temps nécessaire pour la désintégration de la moitié du nombre de noyaux d'échantillons.
le temps nécessaire pour la désintégration de la moitié du nombre de noyaux d'échantillons.* la relation entre t1/2 et λ
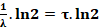
-
4.3. Activité d'un échantillon radioactif :
Activité d'un échantillon radioactif : C'est le nombre de désintégrations par unité de temps :
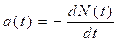 avec
avec 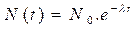 Et donc :
Et donc : 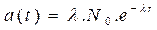 L'unité de
L'unité de 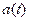 dans S.I. est : Bq (Becquerel). Et on utilise également le Curie :
dans S.I. est : Bq (Becquerel). Et on utilise également le Curie : 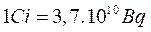
nous mettons :
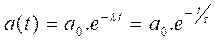 avec
avec 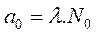

Remarque: La radioactivité est mesurée par des compteurs tels que le compteur "Geiger"
-
-
4. datation par radioactivité :
-
datation Avec du carbone (14) par example :
* Dans l'atmosphère le niveau de Carbone 14 reste constant, avec la nutrition et la respiration, l'organisme échange du Carbone avec le l'enverenement, ce qui rend constante la proportion de Carbone 14 qu'il contient
* Lorsque les êtres vivants meurent, l'échange s'arrête et le niveau de carbone
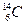 diminue en raison de la désintégration des noyaux
diminue en raison de la désintégration des noyaux 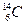 Selon l'équation suivante:
Selon l'équation suivante: 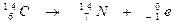
On considère que l'arret de l'échange de carbone avec l'environnement (mort de l'organisme) est l'origine pour les dates t=0s
On prend une masse m de l'élément qui on veu déterminé son âge (mort) et on détermine son activité a (t)
On prend la même masse m de l'élément vivant et nous définissons son activité a0 qui correspond à l'activité de l'élément mort quand il était vivant
et par application de la loi de décroissance radioactive
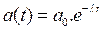 Nous trouvons :
Nous trouvons :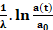
et Par conséquent, l'intervalle de temps entre la date du décès (t0=0) et La date t à laquelle la datation a été faite est : Δt =t-t0=t
Remarque: cette méthode est utilisée pour dater des échantillons qui ne datent pas de plus de 40000 ans . (Parce que les spécimens à plus longue durée de vie contiennent une très petite quantité de
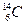 )
)
-