التحولات الكيميائية التي تحدث في منحيين
1. Réactions acide-base: (rappel):
-
1.1. Définitions
Acide : Un acide est, selon Bronstedt, chaque espèce chimique qui est capable de perdre un proton H+ lors d'une réaction chimique. la base : une base est , selon Bronstedt, chaque espèce chimique qui est capables d'acquérir un proton H+ lors d'une réaction chimique .
couples Acide/Base : HA/A- : Le couple acide/base est constitué d'un acide A et de sa base conjuguée A-. la demi-equation : On associe un couple acide / base a une demi-équation :
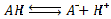 qui modélise le passage d'un acide a sa base conjuguée (ou l'inverse) par la perte (ou le gain) d'ion hydrogène H+
qui modélise le passage d'un acide a sa base conjuguée (ou l'inverse) par la perte (ou le gain) d'ion hydrogène H+
-
2.1. La reaction d'acide-base
C'est un transfert de proton H+ entre un acide HA1 et une base A2-.
* dissolution de chlorure d'hydrogène dans l'eau . : H2O + HCl → H3O++Cl- Les deux couples sont : HCl/Cl- : et H3O+/H2O :
-
2. Définition et mesure du pH d'une solution aqueuse :
-
1.2. Définition:
" Le pH d'une solution aqueuse diluée est défini par la relation:
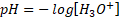 Cette relation équivalente à :
Cette relation équivalente à : 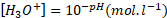 ".
".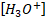 : La concentration d'ions oxonium dans la solution par
mol.L-1.
: La concentration d'ions oxonium dans la solution par
mol.L-1. -
2.2. mesure du pH d'une solution aqueuse :
par pH-mètre Par papier pH par des indicateur colorés  Un appareil qui permet de mesurer directement le pH d'une solution avec précision. Il se compose d'une électrode sensible aux ions H3O+ connectée à un voltmètre numérique marqué en pH.
Un appareil qui permet de mesurer directement le pH d'une solution avec précision. Il se compose d'une électrode sensible aux ions H3O+ connectée à un voltmètre numérique marqué en pH.
 Papier spécial qui change de couleur après avoir été mouillé avec la solution, et nous comparons sa couleur avec l'échelle de couleurs de référence accompagnée des valeurs de pH correspondant à chaque couleur
Papier spécial qui change de couleur après avoir été mouillé avec la solution, et nous comparons sa couleur avec l'échelle de couleurs de référence accompagnée des valeurs de pH correspondant à chaque couleur
 Substances organiques qui changent de couleur en fonction du pH de la solution
Substances organiques qui changent de couleur en fonction du pH de la solution
-
3. Transformations totales et non totales :
-
1.3. Taux d’avancement final:
" Le taux d’avancement final pour une réaction chimique est le quotient de l’avancement finale
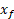 pour une réaction sur son avancement maximal
pour une réaction sur son avancement maximal 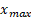 " :
" : 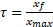
1.3. Transformations totales et non totales:
* Transformations totales (complètes) : Une transformation est dite totale lorsqu'elle se termine par la disparition d'un des réactifs (le réactif limitant) Et alors la relation xf=xm est remplie Et donc τ=1 ou τ=100% Le réactif limitant a réagi complètement
* Transformations non totales (limitées) : On dit que la transformation n'est pas totale (est limitées) lorsqu'elle arrive à son etat final sans que les réactifs disparaissent complètement Et alors la relation xf<xm est remplie Et donc τ<1 اي τ<100% Le réactif limitant n'a pas complètement réagi
-
4. État d'équilibre d'une ensemble chimique :
-
- Interprétation Microscopique de l'Equilibre Dynamique : (Spécifique aux Sciences Mathématiques (A et B) et aux Sciences Physiques):
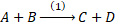
Les quantités de A et B diminuent, donc le nombre de collisions effectives entre elles diminue, ce qui entraîne une diminution de la vitesse
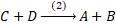
Les quantités de C et D augmentent et donc le nombre de collisions entre elles augmente, ce qui conduit à une augmentation de la vitesse de la réaction en sens inverse (2).
Lorsque les vitesses v1 et v2 sont égales, par exemple, la quantité de réactif A consommée dans la réaction directe (1) est égale à sa quantité formée lors de la réaction dans l'inverse (2), et donc les concentrations molaires du groupe restent constantes dans le temps.
"Dans le cas de l'équilibre d'une ensemble chimique, à chaque instant le nombre de particules qui disparaissent du fait de la réaction dans le sens direct est égal au nombre de particules qui se forment du fait de la réaction dans le sens opposé."
-