حالة توازن مجموعة كيميائي
1. Quotient de réaction Qr :
1.1. Définition :
Soit une transformation chimique d’équation :
a A(aq) + b B(aq) ⇄ c C(aq) + d D(aq)Où A, B, C, D sont les espèces chimiques (réactifs et produits), et a, b, c, d leurs coefficients stœchiométriques.
Le quotient de réaction associé à cette équation est donné par la relation :
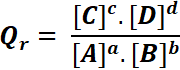
- Qr : grandeur sans dimension.
- [A], [B], [C],[D] : concentrations effectives en mol.L-1 .
- [Xi] = 1 si Xi est un solide non dissous
-[H2O]=1 dans le cas d’une solution aqueuse (H2O solvant)
1.2. Exemples :
CH3COOH(aq) + H2O(l) ⇄ CH3COO-(aq) + H3O+(aq) : Qr,t= ([CH3COO-]t.[H3O+]t)/([CH3COOH]t)
Cu(s) + 2.Ag+(aq) ⇄ Cu2+(aq) + 2.Ag(s) : Qr,t= ([Cu2+]t)/([Ag+]2t)
2. Quotient de réaction à l’équilibre Qr, éq :
2.1. Définition :
On appelle quotient de réaction à l’équilibre Qr, éq la valeur que prend le quotient de réaction lorsque l’état d’équilibre du système chimique considéré est atteint.
Son expression est :
Qr, éq = ([C]céq.[D]déq)/([A]aéq.[B]béq)
Afin de déterminer Qr, éq , on utilise différentes techniques expérimentales pour mesurer les concentrations à l’équilibre :
- la conductimétrie pour les systèmes faisant intervenir des ions.
- la pH-métrie pour les systèmes faisant intervenir des réactions acido-basiques.
2.2. Détermination de Qr, éq par conductimétrie :
A 25°C, on mesure la conductivité d’une solution d’acide éthanoïque CH3COOH, à l’équilibre.
solution S1 S2 C (mol.L-1) 5,0.10-2 1,0.10-2 σ(S.m-1) 34,3.10-3 1,6.10-2 - l’équation de la réaction entre l’acide éthanoïque et l’eau.
CH3COOH(aq) + H2O(l) ⇄ CH3COO- + H3O+
- La connaissance de la conductivité σ de la solution permet d’en déduire xf et ainsi les concentrations des espèces à l’équilibre, puis Qr, éq.
Le quotient de réaction à l’équilibre s’écrit : Qr, éq = ([CH3COO-]éq.[H3O+]éq)/([CH3COOH]éq)
La conductivité de la solution peut se mettre sous la forme : σ= 𝛌CH3COO- .[CH3COO-] + 𝛌H3O+ . [H3O+]
D’après le tableau d’avancement on a [CH3COO-]éq = [H3O+]éq = xf/V
et [CH3COOH]éq = C - (xf/V)
σ =( 𝛌CH3COO- + 𝛌H3O+ ) . [H3O+]
↔ [H3O+] = [CH3COO-]éq = xf/V = σ/( 𝛌CH3COO- + 𝛌H3O+ )
solution S1 S2 C (mol.L-1) 5,0.10-2 1,0.10-2 Qr, éq 1,57.10-5 1,57.10-5 Conclusion :
Pour une transformation chimique donnée, la valeur de Qr, éq est constante, elle ne dépend pas de la composition initiale du système chimique
3. Constante d’équilibre K:
3.1. Définition :
On associe à chaque réaction d’équation : a A (aq) + b B (aq) ⇄ c C (aq) + d D (aq) , une constante K appelée constante d’équilibre telle que : Qr, éq=K.
- La valeur de K ne dépend pas de l’état initial du système, elle dépend uniquement de la température
- A chaque équation de réaction on associe une constante d’équilibre K .
3.2. Exemple :
L’équilibre des acides avec l’eau est caractérisé par leur constante d’équilibre Ka = K.
HCOOH(aq) + H2O(l) ⇄ HCOO-(aq) + H3O+(aq) ; Ka = 1,6.10–4
CH3COOH(aq) + H2O(l) ⇄ CH3COO-(aq) + H3O+(aq) ; Ka = 1,7.10–5
C6H5COOH(aq) + H2O(l) ⇄ C6H5COO-(aq) + H3O+; Ka = 6,8.10–5
4. Facteurs agissants sur le taux d’avancement final:
4.1. Influence de l’état initial du système sur le taux d’avancement final :
On détermine τ le taux d’avancement final pour deux solutions d’acide méthanoïque de concentrations différents on trouve :
- Pour une solution de concentration C1=10,00. 10-3mol.L-1 on a τ1 =1,26%
- Pour une solution de concentration C2= 5,00. 10-3mol.L-1 on a τ2 =17,3%
Conclusion :
C1 > C2 mais τ1 < τ2 , la valeur de τ dépend de l’état initial du système , elle augmente avec la dilution.
4.2. Influence de la constante d’équilibre sur τ.
On détermine τ pour trois solutions d’acides différents de même concentration initiale C=5,00 .10-3mol.L-1.
Les résultats sont donnés dans le tableau suivant :
Solution éthanoïque méthanoïque K 1,6.10-5 1,8.10-4 τ 5,48% 17,3% Conclusion :
La valeur de τ augmente lorsque la valeur de K augmente
Le taux d’avancement final d’un système à l’équilibre, lui, dépend des conditions initiales et de la valeur de la constante d’équilibre.
Remarque :
une réaction peut être considérée comme quasi-totale si son taux d’avancement final est supérieur à 99 %.
Comme τ dépend de K mais aussi des conditions initiales, il n’est pas possible de donner un critère universel portant seulement sur K et prédisant qu’une réaction sera totale
Toutefois, dans la plupart des cas abordés dans notre étude, une réaction dont la constante d’équilibre est supérieure à 104 peut être considérée comme totale .