التحولات المرتبطة بالتفاعلات الحمضية القاعدية في محلول مائي
1. L'autoprotolyse de l'eau :
1.1. Autoprotolyse de l'eau
* La mesure de la conductivité de l'eau distillée(qui à priori ne contient pas d'ions) à 25°C, donne σH2O = 5,5 . 10-6S.m-1.
* L’eau H2O est:
- une base pour le couple H3O+(aq)/H2O(l)
- et un acide pour le couple H2O(l)/OH-(aq)
L’eau, espèce amphotère (ampholyte), joue donc un double rôle d’acide et de base, selon l’équation :
2 H2O(l) ⇄ H3O+(aq) + OH-(aq)
Cette réaction est appelée autoprotolyse de l’eau
* On considère 1,0 L d’eau.
tableau d’avancement :
Equation de la réaction 2 H2O(l) ⇄ H3O+(aq) + OH-(aq) Etat Avancement Quantités de matières en mol Etat initial 0 n 0 0 en cours de transformation x n-2x x x Etat final xf n-2xf xf xf Quantité de matière initiale n :
n = m/Meau =μ0 .V /Meau
μ0=1000 g.Lμ-1 la masse volumique de l' eau
n = 1000 * 1 / 18 = 56 mol
Détermination de xmax:
Le réactif limitant est H2O(l) .
n - 2xmax = 0
xmax = n /2 = 56 /2 = 28 mol
Détermination de xf :
D’après le tableau d’avancement :
xf = nf(H3O+) = [H3O+]f * V
xf = 10-pH * V = 10-7 mol
Détermination de τ :
τ = xf/xmax= 10-7/28 = 3,6.10 -9; très petit devant 1.
La réaction d’autoprotolyse de l’eau est une transformation très limitée .
1.2. Produit ionique de l'eau :
Le produit ionique de l'eau est la constante d'équilibre associée à l'équation d'autoprotolyse de l'eau. Cette constante est notée Ke.
Ke = [H3O+].[HO-]
Ke s'exprime sans unité et les concentrations sont exprimées en mol.L-1 .
* La constante d'équilibre est indépendante de l'état initial (de la concentration initiale) et ne dépend que de la température.
* Ke croît lorsque la température augmente): Pour toute solution aqueuse à 25°C, Ke = 1,0 . 10-14.
Température (°C) 0 25 50 100 Ke 0,10 .10 - 14 1,0.10 - 14 5,5.10 - 14 55.10 - 14 pKe = - log(Ke) 15 14 13,3 12,3 Remarque :
On note pKe = - log(Ke)
pKe = 14 à 25°C .
1.3. Relation entre pH et [HO-]
On prend le logarithme de la relation Ke = [H3O+].[HO-] .
log(Ke) = log([H3O+]) + log([HO-]) Donc pKe = pH – log([HO-])
pH = pK e + log([HO-] = 14 + log([HO-]
[HO-] = 10(pH-14)
1.4. pH des solutions aqueuses :
Le pH des solutions aqueuses usuelles s'étend de 0 à 14.
solution aqueuse acide solution aqueuse neutre solution aqueuse basique [H3O+]>[HO-]
[H3O+].[H3O+]>[HO-].[H3O+]
[H3O+]2 > Ke
-log([H3O+]2 ) < -log(Ke)
[H3O+]=[HO-]
[H3O+].[H3O+]=[HO-].[H3O+]
[H3O+]2 =Ke
-log([H3O+]2 ) = -log(Ke)
[H3O+]<[HO-]
[H3O+].[H3O+]<[HO-].[H3O+]
[H3O+]2 < Ke
-log([H3O+]2 ) > -log(Ke)
A 25°C ; pH < 7 A 25°C ; pH=7 A 25°C ; pH>7
2. Constante d'acidité KA :
2.1. Constante d'acidité KA:
La constante d'acidité KA est la constante d'équilibre associée à l'équation de la réaction d'un acide avec l'eau.
L'équation de la réaction: AH(aq) + H2O(l)(l) = A-(aq) + H3O+(aq)
constante d'acidité : KA = ( [A-(aq)] * [H3O+(aq)] ) / [AH(aq)]
pKA est défini par la relation : pKA = - log(KA) ou KA = 10-pKA
2.2. Exemple :
Couple KA pKA H3O+(aq)/H2O(l) 1 0 HCOOH(aq)/HCOO-(aq) 1,80 . 10-4 3,7 CH3COOH(aq)/CH3COO-(aq) 1,58 . 10-5 4,8 NH4+(aq) / NH3 (aq) 6,3 . 10-10 9,2 H2O(l) / HO-(aq) 10 . 10-14 14 2.3. Relation entre pH et pKA :
On considère un couple acide/base suivante : AH(aq)/A-(aq)
La constante d'acidité associée à le couple est KAest : KA = ( [A-(aq)] * [H3O+(aq)] ) / [AH(aq)]
-log(KA) = -log( ( [A-(aq)] * [H3O+(aq)] ) / [AH(aq)] )
-log(KA) = -log([A-(aq)] / [AH(aq)] ) -log( [H3O+(aq)] )
pKA = -log([A-(aq)] / [AH(aq)] ) + pH
pH=pKA+ log([A-(aq)] / [AH(aq)] )
3. Diagramme de prédominance des espèces acido-basiques . 1- Cas de couple AH (aq) /A - (aq) :
3.1. Définition :
Une espèce A est prédominante par rapport à une espèce B si : [A] > [B]
* Pour déterminer les domaines de prédominance en fonction du pH, on cherche la relation donnant le rapport [B]/[A] en fonction de pH d'une solution aqueuse contenant un acide A et sa base B :
pH = pKA+ log([B]éq /[A]éq )
log([B]/[A]) = pH - pKA alors
* Il y a trois situations possibles :
a- Acide prédomine par rapport à Base : [A] > [B] ([AH] > [A-])
Alors [B]/[A] < 1 ⟺ 10pH-pKA < 1
C'est-à-dire pH - pKA < 0 ⟺ pH < pKA
Si pH < pKA alors l'acide AH prédomine par rapport à Base A -
b- La concentration de l'acide égale à la concentration de la base : [A] = [B] ([AH] = [A-])
Alors ⟺
C'est-à-dire ⟺
Si pH = pKA alors aucune des deux formes ne prédomine.
c- Base prédomine par rapport à Acide : [AH] < [A - ]
Alors ⟺
C'est-à-dire ⟺
Si pH > pKA alors la base A- prédomine par rapport à l'acide AH
* Domaines de prédominance :
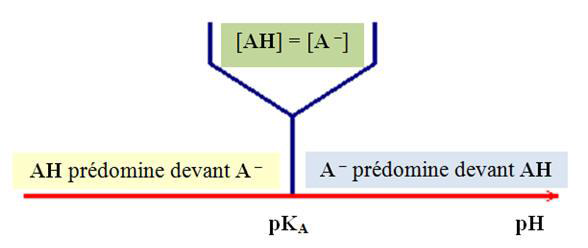
* Distribution des espèces acido-basiques
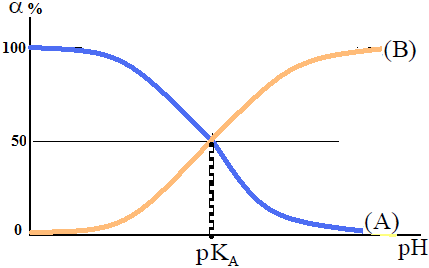
3.2. Cas d'indicateurs colorés :
Un indicateur coloré est un couple acide/base note IndH(aq)/Ind-(aq) , dont la forme acide InH(aq) et la forme basique In-(aq) ont des couleurs différentes en solution.
La constante d'acidité KA,Ind = ( [Ind-(aq)] * [H3O+(aq)] ) / [IndH(aq)]
donc pH=pKA,Ind +log([Ind-(aq)] / [IndH(aq)] )
* On admet que la solution dans laquelle se trouve l'indicateur a la couleur de la forme acide InH si [ IndH ] > 10 [Ind-]
donc log( [Ind-(aq)] / [IndH(aq)] ) < -1
pKA,Ind + log([Ind-(aq)] / [IndH(aq)]) < pKA,Ind -1
pH < pKA,Ind -1
* On admet que la solution dans laquelle se trouve l'indicateur a la couleur de la forme base Ind- si [Ind-] > 10 [ IndH ]
donc log([Ind-(aq)] / [IndH(aq)]) >1
pA,Ind + log([Ind-(aq)] / [IndH(aq)]) > pA,Ind +1
pH > pKA,Ind +1
* La solution prendra une couleur appelée teinte sensible (mélange des couleurs dues à la forme acide et à la forme basique) si [IndH] et [Ind-] sont du même ordre de grandeur, donc si : pKA,Ind -1<pH<pKA,Ind +1.
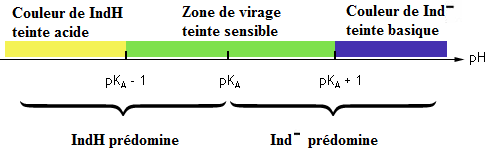
Exemples :
Indicateur Couleur pK Alnd Zone de virage Acide Base Hélianthine Jaune orangé rouge 3,7 3,1 – 4,4 Vert de Bromocrésol jaune bleu 4.7 3.8 - 5.4 Rouge de Méthyle jaune rouge 5.1 4.8 - 6.0 Bleu de Bromothymol jaune bleu 7.0 6.0 - 7.6 phénolphtaléine incolore rose-violet 9.4 8.2 - 10.0
4. Constante d'équilibre associée à une réaction acido-basique
Soit une réaction acido-basique entre l'acide A1H(aq) d'un couple A1H(aq)/A1-(aq) de constant d'acidité KA1 et la base A2-(aq) d'un couple A2H(aq)/A2-(aq) de constant d'acidité KA2.
Equation de la réaction : A1H(aq) + A2-(aq) ⇄ A1-(aq) + A2H(aq)
Constante d'équilibre : K = ([A1-(aq)] * [A2H(aq)] * [H3O+(aq)]) / ([A1H(aq) * [A2-(aq)] * [H3O+(aq)])
Avec KA1= ([A1-(aq)] * [H3O+(aq)]) / [A1H(aq)]
et KA2 = ([A2-(aq)] * [H3O+(aq)]) / [A2H(aq)]
Donc K = ([A1-(aq)] * [A2H(aq)] * [H3O+(aq)]) / ([A1H(aq)] * [A2-(aq)] * [H3O+(aq)])
Finalement K = KA1 / KA2 = 10pKA2-pKA1
Exemple :
L' équation de réactions entre l’acide éthanoïque et l’ammoniac est
CH3COOH(aq) + NH3(aq) ⇄ NH4+(aq) + CH3COO-(aq)
La constantes d’équilibre associée à la réaction
K = Qr,eq = [CH3COO-]eq [NH4+]eq / [CH3COOH]eq [NH3]eq
K = KA1 / KA2
La valeur de la constante :
CH3COOH(aq)/CH3COO-(aq) ; pKA1 = 4,7
NH4+(aq)/NH3(aq) pKA2 = 9,2
donc K=3,1.104
5. Comparaison du comportement en solution des acides entre eux et des bases entre elles :
5.1. Cas des acides :
Considérons deux solution acide de même concentration C=1 . 10-2 mol/L
Solution acide pKA KA pH τ final d'méthanoïque HCOOH pKA1 = 3,7 KA1 =2,0 . 10-4 pH1 = 2,9 τ1 =13 % d'acide éthanoïque CH 3 COOH pKA2 = 4,8 KA2 =1,6 . 10-5 pH2 = 3,4 τ2 =4 % KA est donc une fonction croissante de τ.
Pour la meme concentration C, plus KA est grand (pKAest plus petit), plus l'acide AH est dissocié, plus le pH de la solution est faible et plus le taux d'avancement τ de la réaction est plus grand
5.2. Cas des bases :
Considérons deux solution basique de même concentration C=1 . 10-2 mol/L
Solution basique pKA KA pH τ final Ammoniaque NH 3 pKA1 = 9,2 KA1 = 6,3 . 10-10 pH1 = 10,6 τ1 =4 % Méthylamine CH 3 NH pKA2 = 10,7 KA2 = 2 . 10-11 pHτ2 = 11,4 τ2 =25 % Pour la meme concentration C, plus KA est faible, plus la base est dissocié, plus son pH est grand et plus le taux d'avancement τ de la réaction est grand.
Conclusion :
chaque acide plus fort est associée une base plus faible et vice versa