التطور التلقائي لمجموعة كيميائية
1. Rappel - quotient de réaction :
1.1. quotient de réaction :
le quotient de réaction
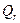 associé à l'équation :
associé à l'équation :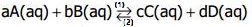
est défini par l'expression :
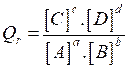
1.2. quotient de réaction à l'équilibre :
Dans le cas d'un groupe chimique en équilibre, le quotient de réaction
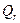 prend une valeur qui n'est pas liée à l'état initial du système chimique ; C'est la constante d'équilibre
prend une valeur qui n'est pas liée à l'état initial du système chimique ; C'est la constante d'équilibre
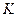 Où :
Où : 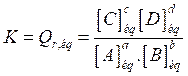
2. Critère de l'evolution spontanée :
une comparaison du quotient de réaction
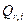 avec la constante d'équilibre
avec la constante d'équilibre
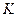 assossiée à l'équation de réaction
permet de prédire le sens d'évolution spontanée dans chaque mélange.
assossiée à l'équation de réaction
permet de prédire le sens d'évolution spontanée dans chaque mélange. où :
" Un système chimique évolue spontanément vers un état d'équilibre de sorte que le quotient de la réaction
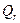 converge à la constante d'équilibre
converge à la constante d'équilibre 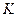 ".
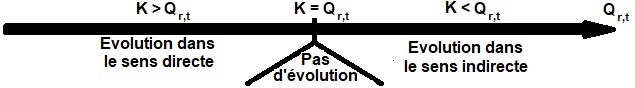
".Nous distinguons trois cas :
si K > Q r,t Le système chimique évolue dans le sens directe (1) jusqu'à ce qu'il atteigne l'état d'équilibre
si K = Q r,t état d'équilibre du système chimique
si K < Q r,t Le système chimique évolue dans le sens opposé (2) (indirecte, inverse) jusqu'à ce qu'il atteigne l'équilibre