التـحـولات التـلـقـائيـة في الأعـمـدة وتحـصـيـل الطـاقـة
1. Le transfert spontané d'électrons :
1.1. Transfert spontané direct (entre différentes espèces chimiques) :
Dans le cas de la présence de l'oxydant et du réducteur dans le même milieu, le transfert des électrons s'effectue de manière directe
1.2. quotient de réaction à l'équilibre :
Dans le cas où l'oxydant et le réducteur ne sont pas présents dans le même milieu, le transfert d'électrons s'effectue en liant le réducteur à l'oxydant : transfert de manière indirecte
2. Composants de la pile :
- La pile est un générateur électrique qui convertit l'énergie chimique résultant d'une réaction redox spontanée en énergie électrique.
- Une pile est constituée de deux moitiés ; deux demi-piles
- Chaque demi-pile contient un couple oxydant et réducteur : nous appelons une demi-pile un groupe constitué d'un fil (ou d'une plaque) de métal M(s) , appelée électrode, immergée dans une solution d'électrolyte contenant des ions Mn+(aq)
- Ils sont reliés électriquement par un pont salin (ionique)
3. Principe de fonctionnement de la pile :
3.1. Exemple: Pile de DANIEL .
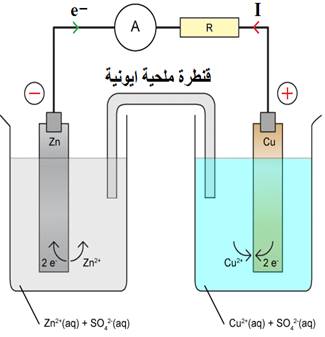
* La première demi-pile
au niveau du pôle négatif de la pile : l'anode (-) Zn
La demi-équation de l'oxydation se produit : Zn(s) ⇄ Zn2+(aq) + 2e-
et cela conduit à :
- La production des ions cations : c'est-à-dire une augmentation du nombre de charges positives.
- La libération d'électrons qui se propagent à travers le fil et atteignent la seconde demi-pile.
Un excès de charge positive et un déficit de charge négative
* La seconde demi-pile
au niveau du pôle positif de la pile : la cathode (+) Cu
La demi-équation de la réduction se produit : Cu2+(aq) + 2e- ⇄ Cu(s)
et cela conduit à :
- Consommation d'ions : c'est à dire une diminution du nombre de charges positives.
- Consommation d'électrons qui arrivent de la première moitié de la pile.
Un excès de charge négative et un déficit de charge positive
* Pont salin ionique
Le pont salin permet de connecter les deux demi-piles, assurant la neutralité électrique, car le nombre de charges positives est égal au nombre de charges négatives.
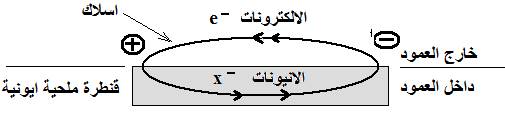
3.2. Déterminer la polarité de la pile
Méthode 1 : Utilisation de l'ampèremètre (ou du voltmètre), où si l'appareil indique une valeur positive, cela signifie que son pôle négatif COM est relié au pôle négatif de la pile, mais si l'appareil indique une valeur négative, cela signifie que son le pôle négatif COM est relié au pôle positif de la pile.
Méthode 2 : Selon les observations expérimentales, la plaque dans laquelle la corrosion est observée signifie qu'elle a été soumise au processus d'oxydation, c'est-à-dire qu'elle représente le pôle négatif de la pile, et sur la plaque dans laquelle le dépôt est observé, cela signifie que la réaction de réduction s'est produite à côté, c'est-à-dire qu'elle représente le pôle positif de la pile.
Méthode 3 : En adoptant le critère d'évolution spontanée, où le véritable sens de l'évolution du groupe chimique est déterminé, puis l'équation est décomposée en deux moitiés, donc l'oxydation correspond au pôle négatif et la réduction correspond au pôle positif.
3.3. Schéma conventionnel d'une pile
On considère une pile composée des deux couples
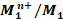 et
et
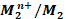 où
où
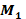 pôle (-) et
pôle (-) et
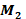 pôle (+).
pôle (+). En général, le schéma conventionnel (la représentation idiomatique) de cette pile est :
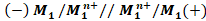 Les deux lignes parallèles // indiquent un pont ionique salin.
Les deux lignes parallèles // indiquent un pont ionique salin.Exemple de pile de DANIEL :
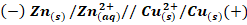
4. Etude quantitative d'une de la pile :
4.1. La quantité d'électricité
* On appelle la quantité d'électricité Q Utilisé pendant l'exécution d'une pile pour une periode Δt , la valeur absolue de la charge totale des électrons échangés durant cette période : Q=N.e
où N est le nombre d'électrons échangés pendant
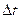 le temps de travail de la pile et e est la charge initiale de l'électron
le temps de travail de la pile et e est la charge initiale de l'électronavec N=n(e-).NA
Nous concluons que : Q= n(e-).NA.e = n(e-).F
Avec la quantité : F = NA.e est appelée constante Faraday et représente la charge de 1 mole d'électrons.
* Si I l'intensité du courant dans le circuit est constant sur une période Δt, on écrit : Q = I.Δt
Donc : Q = I.Δt= n(e-).F
4.2. La quantité maximale d'électricité pouvant passer par une extrémité d'un poteau :
Lorsque la pile atteint l'équilibre, les quantités d'espèces interférentes cessent d'évoluer, aucune interaction ne se produit au niveau des deux électrodes et donc il n'y a pas de transfert d'électrons à travers le circuit extérieur : la pile ne peut plus générer de courant,
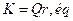 et
et 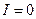 .
. "la pile, lorsqu'elle est en équilibre, est tellement usée qu'ellz ne peut pas générer de courant électrique."
La quantité maximale d'électricité qui peut être passée à travers une pile, c'est-à-dire la capacité de la pile :
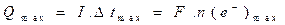
où
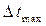 Vie de la pile.
Vie de la pile. 4.3. La quantité d'électrolyte et l'avancement de la réaction pendant le fonctionnement de la pile Δt
Tableau descriptif pour l'une des deux demi-équations.
Red ⇄ Ox + n e-
à t=0
n0(Red)
n0(Ox)
0
à t
n0(Red)-x(t)
n0(Ox)+x(t)
n.x(t)
apartir de tableau descriptif : n(e-)=n.x(t) où n est le nombre d'électrons
Q= n.x(t).F
Autrement dit, x(t) =
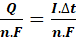
5. Exemples des piles courantes :
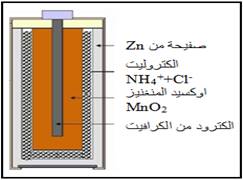
5.1. La pile salin : Leclanche :
Il est appelé salin car ses électrodes sont immergées dans une faible solution de chlorure d'ammonium, NH4++Cl-) et chlorure de zinc ( .
- L'équation exprimant son travail.
Zn+2MnO2+2H+ DZn2++2MnO(OH)
- Représentation idiomatique :
(-) Zn/Zn2+//MnO(OH)/MnO2/C (+)
5.2. La pile alvéolaire :
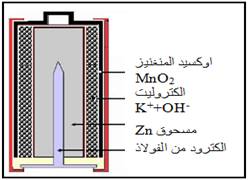
- Presque les mêmes composants de la pile de sel sauf que les deux électrodes sont immergées dans une solution basique tamponnée d'hydroxyde de potassium (K++OH- ), et il est appelé alcalin à cause de l'élément potassium.
- L'équation exprimant son fonctionnement :
Zn+2MnO2+2OH-+2H2O ⇄ Zn(OH)4 2-+2MnO(OH)
- représentation idiomatique :
(-)Zn/Zn(OH)42-//MnO(OH)/MnO2/acier (+)
5.3. La pile a combustible :
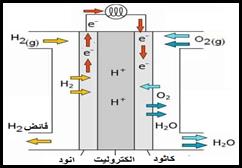
Comme les piles avec du dihydrogène et du dioxygène
- H2 atteint l'anode et il est oxydé
- O2 atteint la cathode et il est réduit
L'électrolyte utilisé représente un pont ionique et est soit basique (K++OH-) ou acide de type (acide phosphorique)
Équation de fonctionnement de la pile
2H2 + O2 ⇄ 2H2O