تـفــاعـلات الأسـتـرة والحـلـمـأة
1. Réaction d'estérification :
1.1. Définition:
La réaction d'estérification est une réaction qui se produit entre un acide carboxylique et un alcool au cours de laquelle l'acide carboxylique perd le groupe (-OH), tandis que l'alcool perd (-H). Ainsi, les deux molécules s'unissent pour donner un ester et une molécule d'eau selon à l'équation suivante :
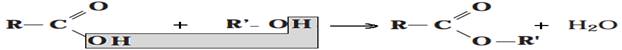
1.2. Caractéristiques de la réaction d'estérification :
Interaction thermique : c'est-à-dire que le groupe n'échange pas de chaleur avec le milieu extérieur
Réaction lente : il faut beaucoup de temps pour arriver à son point (heures....)
Réaction limitée : atteint la fin avec les réactifs présents ensemble
2. Réaction d'hydrolyse
2.1. Définition :
C'est une réaction qui se produit entre un ester et l'eau, c'est-à-dire dans le sens inverse de la réaction d'estérification, selon l'équation suivante R

2.2. Caractéristiques de la réaction d'hydrolyse :
Interaction thermique : c'est-à-dire que le groupe n'échange pas de chaleur avec le milieu extérieur
Réaction lente : il faut beaucoup de temps pour atteindre sa limite
Réaction limitée : atteint la fin avec les réactifs présents ensemble
3. L'équilibre estérification-hydrolyse
- Les réactions d'estérification et d'hydrolyse sont simultanées et se produisent dans des sens opposés.
- En général on exprime l'équilibre estérification-hydrolyse par l'équation
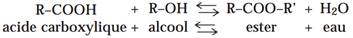
L'eau joue un rôle réactif dans l'hydrolyse et l'estérification, et n'est pas un solvant.
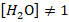
- L'expression hors réaction pour une réaction d'estérification est:
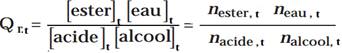
- l'expression de L'équilibre de la réaction d'estérification est:
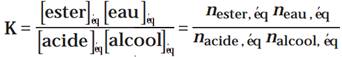
En partant d'un mélange de moles égales n 0 de l'acide et n 0 de l'alcool, alors à l'équilibre on obtient la quantité d'ester en fonction du type d'alcool utilisé
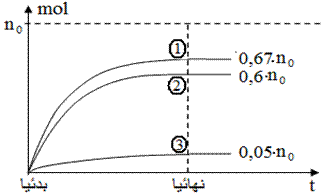
alcool primaire 1, alcool secondaire 2, alcool tertiaire 3
4. Contrôle d'une transformation chimique
Afin d'atteindre l'état final dans un délai plus court, le taux de développement du système chimique doit être augmenté
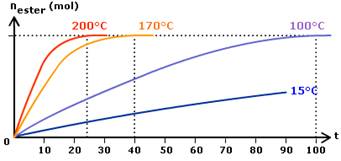
4.1. En augmentant la température
Plus la température du système chimique est élevée, plus son évolution est rapide
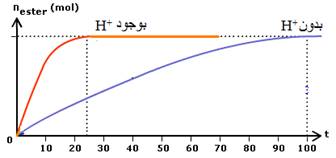
4.2. En ajoutant un catalyseur :
un catalyseur est une espèce chimique qui augmente la vitesse de réaction sans interférer avec les réactifs dans l'équation de réaction
La présence du catalyseur accélère l'évolution du système chimique
5. Rendement de la transformation chimique
5.1. Définition du rendement
Le rendement r d'une réaction chimique est égal au résultat de la division de la quantité de substance n exp obtenue expérimentalement, sur la quantité de substance n th que l'on s'attend à obtenir compte tenu de la transformation totale, et on écrit r =
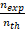 et la connaissance de sa valeur permet l'évaluation de l'efficacité de la transformation.
et la connaissance de sa valeur permet l'évaluation de l'efficacité de la transformation. 5.2. Quelques façons d'augmenter le rendement
Pour augmenter le rendement de la fabrication des esters, par exemple, nous :
- En utilisant un des réactifs (un acide ou un alcool) en abondance
- Éliminer l'un des produits (l'eau ou l'ester formé) car on évite la transformation en sens inverse