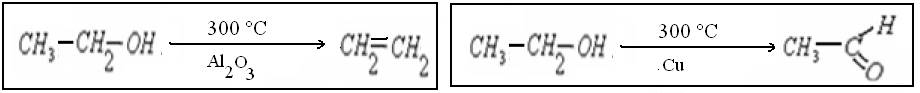
التحكم في تطور المجموعة الكيميائية.
1. Pourquoi le changement d'un réactif
Lors de chaque processus de fabrication, les éléments suivants sont observés :
* La productivité (le rendement) de fabrication doit être élevée tout en préservant l'énergie et les matières premières.
* Le coût de production doit être faible
* Vitesse de productivité
Pour ces raisons... des conditions appropriées doivent être fournies (satisfait, remplies) en changeant les réactifs, les additifs de catalyseur ou ...
-
2. Contrôle de l'évolution d'un système chimique en changeant un réactif.
1.2. Fabrication d'un Ester
La fabrication d'esters à partir d'un acide carboxylique et d'un alcool se caractérise par des réactions lentes et non totales qui conduisent à la formation d'eau, donc l'ester est hydrolysé.
On remplace l'acide carboxylique par l'un de ses dérivés, comme l'anhydride d'acide carboxylique
Équation de la réactions (transformation)
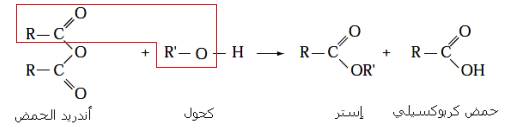
* Ces réactions se caractérisent par leur rapidité et leur achèvement complet (total).
* Réaction en milieu anhydre pour éviter la dissociation de l'acide nucléique et prévenir l'apparition et la confiance de l'hydrolyse
Exemple :
Synthèse de l'aspirine à partir d'acide éthanoïque et l'acide 2-hydroxybenzoïque entre 60° et 90° à l'aide de catalyseurs (H2SO4) selon l'équation suivante :
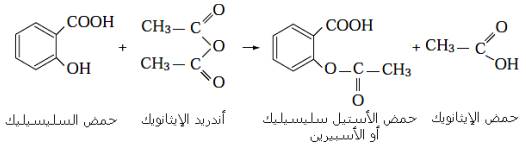
2.2. Hydrolyse basique d'un Ester : Saponification :
L'hydrolyse des esters en présence d'eau se caractérise par le fait qui est une réactions lentes et incomplètes, et elle conduit à la formation d'un acide et d'un alcool, et donc l'estérification se produit.
Pour cette raison, nous changeons (remplaçons) le réactif qui est l'eau par une base forte telle que ( Na++ OH- ) ou ( K+ +OH- ) , selon l'équation suivante :
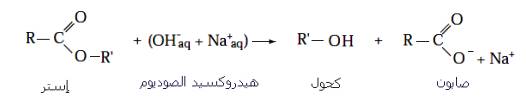
Résultat : le carboxylate de sodium R-COO- + Na+, c'est du savon
3.2. Saponification des liposomes (hydrolyse basique) : préparation du savon
Les corps gras sont des triesters, qui sont le résultat de la réaction d'estérification entre un acide gras et le glycérol.
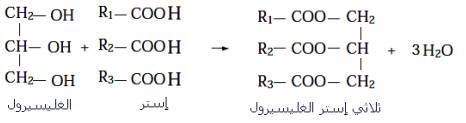
Le savon est préparé en saponifiant les corps gras (liquides et solides), qui contiennent les groupements caractéristiques 'esters' , selon l'équation suivante :
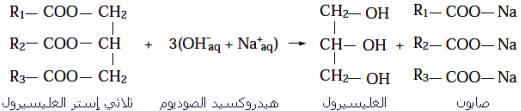
Remarque : Dans le cas de l'utilisation de ( Na+ + OH- ) nous obtenons un savon dur, et dans le cas de l'utilisation de ( K+ + OH- ) nous obtenons un savon mou
L'effet du savon sur la saleté :
La molécule de savon (ion carboxylate R-CO2- ) est constituée de deux parties :
* tête –CO2- : hydrophile et lipophobe .
* queue -R : hydrophobe et Lipophile .
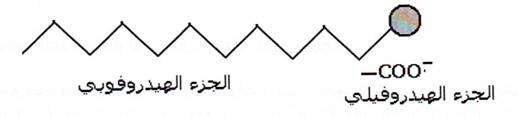
Lorsqu'un vêtement taché de graisse est placé dans de l'eau savonneuse, les fractions Lipophiles s'accumulent (se rassemblent) autour de la tache du lipide.
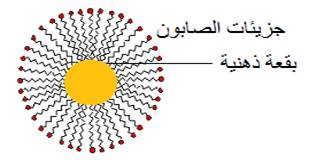
Après le processus de frottement, les taches grasses entourées de particules de savon sont séparées du tissus et sont dispersées dans l'eau
3. Contrôle de l'évolution d'un système chimique par catalyse :
1.3. Définition d'un catalyseur
Le catalyseur est une espèce chimique sélective et spécifique qui ne modifie pas l'état d'équilibre, mais augmente plutôt la vitesse de réaction.
2.3. types des catalyseurs
Catalyse homogène : lorsque le catalyseur et les réactifs sont dans la même phase.
Catalyse hétérogène : lorsque le catalyseur et les réactifs n'appartiennent pas à la même phase.
Catalyse enzymatique : lorsque le catalyseur est une enzyme. Il comprend plusieurs vacuoles (lacunes) qui sont des sites efficaces qui stabilisent les réactifs et augmentent la vitesse de leur réaction
3.3. sélectivité d'un catalyseur
Le catalyseur dirige la transformation chimique, ce qui signifie que la transformation peut progresser dans une direction différente selon le catalyseur utilisé