المقادير المرتبطة بكميات المادة
1. Quantité de matière (rappel)
la mole ( C'est la quantité de matière dans un système contenant un nombre d'entités élémentaires égal au nombre d'atomes présents dans 12g de carbone 12. Qui est 6 ,02 10 23 atome. On l'appelle nombre d'Avogadro . Et son symbole est N A .
Pour un échantillon contenant un nombre N d'entités élémentaires, la quantité de matière pour cet échantillon est n .
![]() où:
où:
![]() (mol)
(mol)
![]() (mol
-1
)
(mol
-1
)
2. Quantité de matière pour les corps solides et liquides
2.1. Quantité de matière et masse
![]() Quantité de matière
n
pour un échantillon dont la masse
m
Composé d'une espèce chimique
X
sa masse molaire
M(X)
est:
(g)
Quantité de matière
n
pour un échantillon dont la masse
m
Composé d'une espèce chimique
X
sa masse molaire
M(X)
est:
(g)
![]()
![]() (mol)
(mol)
![]()
(g.mol -1 )
Exercice d'application::
Nous mesurons une masse m 1 = 100 g d'eau pure et aussi une masse m 2 = 100 g de fer.
1. Calculer la quantité de molécules d'eau dans la masse m 1 .
2. Calculer la quantité d'atomes de fer dans la masse m 2 .
2.2. Quantité de matière et volume
2.1.a. masse volumique et densité
![]() (g)
(g)
*
![]()
![]() La masse volumique est exprimée par la relation:
La masse volumique est exprimée par la relation:
![]() (g.m
-3
)
(g.m
-3
)
(m -3 )
*
Densité d'un corps avec une masse volumique
![]() par rapport à un corps de référence avec une masse volumique
par rapport à un corps de référence avec une masse volumique
![]() est:
est:
![]() n'a pas d'unité.
n'a pas d'unité.
REMARQUE:
Pour les corps solides et liquides, on choisit l'eau comme corps de référence.
![]() .
.
b. Relation entre la quantité de matière et le volume
la quantité de matière
n
d'un'échantillon d'un volume
V
et sa masse volumique
![]() est calculée par relation:
est calculée par relation:
![]()
Exercice d'application::
le hexane
C
6
H
14
est un liquide à température
20°C
, la masse volumique
![]() .
.
Calculer le volume V de l'hexane qui doit être mesuré avec un testeur gradué pour obtenir n = 0,1 mol de ce liquide.
3. Quantité de matière pour les gaz
3.1. Relation entre la quantité de matière d'une gaz et son volume (rappel)
* le volume molaire V m d'un gaz est le volume occupé par une mole de gaz dans des conditions spécifiques de température et de pression. Son unité est : L.mol -1 .
*
![]() Quantité de matière dans un échantillon de gaz de volume
V
est :
(L)
Quantité de matière dans un échantillon de gaz de volume
V
est :
(L)
![]()
![]()
![]() (mol)
(mol)
(L.mol -1 )
remarque: Dans les conditions standard (t 0 = 0°C ; p 0 = 1 atm) V 0 = 22,4 L.mol -1
3.2. Loi Boyle-Marriott
texte de loi: A température constante, et pour une certaine quantité de gaz le produit P.V reste constant.
3.3.
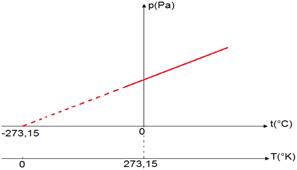 l'échelle absolue de température
l'échelle absolue de température
Nous prenons une certaine quantité de gaz dont le volume reste constant, et étudions l'évolution de la pression P en fonction de température T .
Les résultats expérimentaux ont permis à la ligne de courbe P = f(T) .
La courbe coupe l'axe horizontal à la température -273,15°C C'est une température minimale absolue qui ne peut pas être inférieure à.
Nous déplaçons l'axe des ordonnées au point -273,15 °C Nous obtenons donc ce qu'on appelle la gradation absolue. En substitution de l'axe des températures centigrades (°C) nous utilisons l'axe de température absolu. T . Exprimé par l'unité K (Kelvin) .
![]() La relation entre les degrés Celsius et la température absolue est donc :
(°C)
La relation entre les degrés Celsius et la température absolue est donc :
(°C)
![]() T = t + 273,15
(°K)
T = t + 273,15
(°K)
REMARQUE: la degré celsius de température t = -273,15 °C correspond à T = 0 °K et appelé zéro absolu .
3.4. le gaz parfait
a. modèle du gaz parfait
Le gaz est considéré comme complet si:
* Ses particules sont des boules éparses.
* Ses particules ne s'influencent pas à distance.
* Les collisions entre les molécules de gaz sont toutes élastiques.
REMARQUE:
* Le gaz parfait est entièrement soumis à la loi Boyle-Marriott.
* Les gaz réels, sous faible pression, se comportent comme un gaz parfait.
b. L'équation d'état pour un gaz parfait
L'état d'un gaz est caractérisé par quatre variables, à savoir la pression P , et le volume V , et la température T , Et la quantité de matière n , et on les appelle variables d'état .
Des expériences ont montré que les variables d'état d'un gaz parfait sont liées les unes aux autres par la relation : P.V = n.R.T Équation d'état pour les gaz parfaits.
où R : constante de gaz parfaits . sa valeur:
* R=8,314Pa.m 3 .K -1 .mol -1 lors de l'expression: V(m 3 ) ; T(°K) ; n(mol) ; p(Pa)
* R = 0,082 atm.L.K -1 .mol -1 lors de l'expression: V(L) T(°K) ; n(mol) ; p(atm)
Exercice d'application:
Calculer la quantité de matière d'air dans un ballon dant volume V = 0,5 L dans des conditions normales de température et de pression (p = 1,013 10 5 Pa ; t = 20 °C) .