التركيز والمحاليل الإلكتروليتية
La concentration et les solutions électrolytiques
1. Corps ionique solide
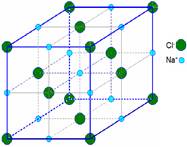 Le corps ionique solide se compose d'ions positifs (cations) et d'ions négatifs (anions) monolithiques dans un arrangement ordonné appelé le Cristal. La cohésion du cristal est due aux effets électrostatiques échangés entre les ions. Mais un solide ionique est toujours électriquement neutre.
Le corps ionique solide se compose d'ions positifs (cations) et d'ions négatifs (anions) monolithiques dans un arrangement ordonné appelé le Cristal. La cohésion du cristal est due aux effets électrostatiques échangés entre les ions. Mais un solide ionique est toujours électriquement neutre.
Exemples:
* chlorure de sodium est constitué d'ions Na + et Cl - qui sont posisionnés selon la règle suivante: (voir figure)
* Le cristal de fluor de calcium est constitué de Ca 2+ et de F - et sa formule s'écrit comme suit : CaF 2 (Substance insoluble dans l'eau) .
2. Le caractère dipolaire d'une molécule
2.1. Élément d'é lectronégativité
Une liaison covalente entre deux atomes résulte du fait que chaque atome partage un électron de sa couche électronique externe.
*  Dans le cas d'une molécule constituée de deux atomes identiques, la paire d'électrons de liaison est située à la même distance entre eux.
Dans le cas d'une molécule constituée de deux atomes identiques, la paire d'électrons de liaison est située à la même distance entre eux.
* Dans le cas d'une molécule constituée de deux atomes différents, l'un d'eux peut attirer plus la paire d'électrons de liaison que le second. Cela se traduit par l'apparition d'une charge partielle négative 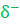 sur l'atome qui attire davantage la paire d'électrons, et d'une charge partielle positive
sur l'atome qui attire davantage la paire d'électrons, et d'une charge partielle positive 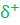 sur l'autre atome. On dit que la liaison covalente est polarisée et la molécule a une caractéristique bipolaire (Caractère dipolaire) .
sur l'autre atome. On dit que la liaison covalente est polarisée et la molécule a une caractéristique bipolaire (Caractère dipolaire) .
* définition
L'électronégativité est la tendance d'un atome d'un élément à attirer la paire de liaisons covalentes qu'il forme avec un autre atome.
Remarque : L' électronégativité des éléments augmente de gauche à droite et de bas en haut dans le tableau périodique des éléments chimiques.
2.2. La caractéristique dipolaire de la molécule de chlorure d'hydrogène
Étant donné que l'atome de chlore est plus électronégatif que l'atome d'hydrogène, la liaison H-Cl est polarisée et nous disons que la molécule de HCl a une caractéristique dipolaire .
2.3. La caractéristique dipolaire de la molécule d'eau
Comme l'atome d'oxygène est plus électronégatif que l'atome d'hydrogène, la liaison HO est polarisée: donc chaque atome d'hydrogène porte une charge partielle 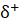 et l'atome d'oxygène porte une charge partielle
et l'atome d'oxygène porte une charge partielle 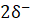 .
.
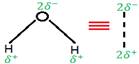
Puisque la molécule d'eau est non linéaire, alors le centre de masse de charge négative n'est pas identique au centre de masse de charge positive, nous disons donc que la molécule d'eau a une caractéristique bipolaire.
3. solution électrolytique aqueuse
1. Définitions
* on obtient une solution en dissolvant un corps solide ou liquide ou gazeux dans un liquide appelé solvant .
* Si le solvant est de l'eau , la solution est appelée solution aqueuse .
* Lorsque la solution contient des ions, on dit que c'est une solution ionique, et comme c'est un conducteur de courant électrique, on dit que c'est une solution électrolytique .
* Objets qui, dissous dans l'eau, dégagent des solutions électrolytiques appelées électrolytes .
Exemples:
* La solution de chlorure de sodium contient des ions : Na + et Cl - .
* la solution d'acide sulfurique contient des ions : H + et SO 4 2- .
* Une solution d'acide chlorhydrique contient des ions : H + et Cl - .
2. Les phases de solubilité des électrolytes dans l'eau
a. étape de dissociation
Lorsqu'un électrolyte est placé dans l'eau, les pôles positifs des molécules d'eau attirent les ions négatifs du cristal ou les atomes les plus électronégatifs du corps moléculaire (ils séparent la paire commune et deviennent anion), tandis que les pôles négatifs des molécules d'eau attirer les ions positifs du cristal ou les atomes moins électronégatifs du corps moléculaire (perdre le co-électron) dans la paire et se transformer en cation).
b. étape d'hydratation
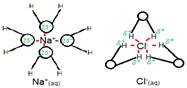 Une fois l'ion libéré du cristal ou de la molécule, il est entouré d'un certain nombre de molécules d'eau, empêchant ainsi l'ion de se recoller. Ce phénomène est appelé hydratation des ions .
Une fois l'ion libéré du cristal ou de la molécule, il est entouré d'un certain nombre de molécules d'eau, empêchant ainsi l'ion de se recoller. Ce phénomène est appelé hydratation des ions .
Pour exprimer l'hydratation des ions, un signe est ajouté (aq) au symbole de l'ion.
Un cas particulier : l' hydratation de l'ion hydrogène H + conduit à sa liaison à une molécule d'eau et s'écrit : H+(aq) ou H3O+(aq) oxonium .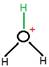
c. phase de dispersion
Cette étape consiste en la diffusion des ions hydratés dans la solution pour devenir homogène. Ce processus peut être accéléré en agitant.
3. Equation de la réaction associée à la dissolution de l'électrolyte
La solubilité d'un électrolyte dans l'eau est un déplacement chimique qui est exprimé par l'équation de réaction de solubilité.
Exemples:
* dissolution du NaCl dans l'eau : NaCl(S)  Na+(aq) + Cl+(aq) et la solution est représentée par : Na +(aq) + Cl-(aq) .
Na+(aq) + Cl+(aq) et la solution est représentée par : Na +(aq) + Cl-(aq) .
* dissolution de H2SO4 dans l'eau : H2SO4 (l)  2H+(aq) + SO42-(aq) et la solution est représentée par : 2H+ + SO42-.
2H+(aq) + SO42-(aq) et la solution est représentée par : 2H+ + SO42-.
* dissolution de HCl dans l'eau ;: HCl(g)  H+(aq) + Cl-(aq) et la solution est représentée par : H+(aq)+ Cl-(aq) . (ou bien : HCl(g) + H 2O(l)
H+(aq) + Cl-(aq) et la solution est représentée par : H+(aq)+ Cl-(aq) . (ou bien : HCl(g) + H 2O(l)  H3O+(aq) + Cl-(aq) et la solution est représentée par : H3O +(aq) + Cl-(aq) .)
H3O+(aq) + Cl-(aq) et la solution est représentée par : H3O +(aq) + Cl-(aq) .)
4. concentrations molaires
1. La concentration molaire du soluté utilisé
La concentration molaire C du soluté A est égale à la quantité de soluté présente dans un litre de solution, exprimée en mol.L-1.
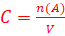
2. La concentration molaire d'un type chimique présent dans la solution
La concentration molaire d'une espece chimique X présent dans une solution est égale à la quantité de matière de cette espece présente dans un litre de solution et est notée par le symbole [X] et exprimée en mol.L-1 .
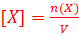
5. Exercice D'application :
On prépare une solution aqueuse de chlorure de plomb, de volume V = 10 mL, en dissolvant une masse de m = 250 mg de plomb chlore PbCl 2 (s) dans l'eau.
1. Calculez la concentration molaire C du soluté utilisé.
2. Écrivez l'équation de dissolution .
3. Calculez les concentrations molaires effectives des ions présents dans la solution.
On donne : M(Pb) = 207,2 g.mol -1 ; M(Cl) = 35,5 g.mol -1