المواصلة والموصلية
-
1. Conductance d'une partie d'une solution électrolytique:
-
1.1. Conductance d'une partie d'une solution électrolytique :
Lorsque deux plaques de cuivre, planes et parallèles, sont immergées dans une solution d'électrolyte, et qu'une tension constante ou alternative est appliquée entre elles, la partie enfermée entre les deux plaques de la solution se comporte comme un dipôle de résistance R et de Conductance G.
où:
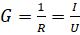
Remarque:
Pour mesurer la conductance d'une partie d'une solution électrolytique, on utilise une tension alternative sinusoïdale avec une fréquence relativement élevée de 500Hz pour éviter les perturbations des réactions chimiques au niveau des deux plaques.
-
2.1. Facteurs affectants la conductance d'une partie d'une solution électrolytique:
a. Facteurs influençants liés aux caractéristiques de la cellule de mesure
* La conductance G est proportionnelle à la surface immergée S des deux plaques de mesure.
* La conductance G est inversement proportionnelle à la distance L entre les deux plaques de mesure.
b. Facteurs influençants liés aux caractéristiques de la solution étudiée
* La conductance G est liée à la nature des ions présents dans la solution.
* La conductance G augmente avec l'augmentation de la température de la solution.
* La conductance G est proportionnelle à la concentration de la solution C.
La courbe représentant la conductance G en fonction de concentration C est appelée courbe d'étallonage, et elle est utilisée pour déterminer les concentrations des solutions d'électrolytes.
Remarque importante:
Pour pouvoir utiliser la courbe d'étallonage G = f(C) pour déterminer la concentration d'une solution, les conditions suivantes doivent être remplies:
* Maintenir la stabilité de tous les autres facteurs influençants.
* Les concentrations des solutions étudiées sont inférieures à 10-2mol.L-1. (A des concentrations plus élevées, la courbe d'étallonage ne conserve pas sa propriété linéaire).
-
-
2. Conductivité de la solution électrolytique:
-
1.2. définition:
La conductivité σ est une caractéristique de l'électrolyte (non liée aux caractéristiques de la cellule de mesure).
La relation de la conductivité σ à la conductance G est:
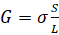
L'unité de conductivité est:(S.m-1)
où: k=S/L : Une grandeur qui caractérise une cellule de mesure est appelée constante de la cellule.
-
2.2. conductivité molaire ionique:
Chaque ion dans une solution est caractérisé par sa taille, sa charge et son état d'hydratation, ce qui affecte sa capacité à conduire le courant électrique, et cette capacité est exprimée par la conductivité molaire ionique. Notée par λ, son unité est : Sm2.mol-1 .
-
3.2.La relation entre la conductivité d'une solution et les conductivités molaires ioniques:
Dans une solution ionique aqueuse, il existe n types d'ions Xi à charge unique, chaque espèce apporte une quantité de : σi=λi.[Xi].
Ainsi, nous écrivons la conductivité de la solution sous la forme suivante:
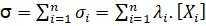
-